در مورد انرژی حرارتی به زبان ساده! مقدار گرما. واحدهای حرارتی گرمای خاص محاسبه مقدار گرمای مورد نیاز برای گرم کردن بدن یا آزاد شده از آن در هنگام سرد شدن چقدر گرما برای متر گرم آب لازم است.
بشر انواع کمی از انرژی را می شناسد - انرژی مکانیکی (جنبشی و پتانسیل)، انرژی درونی (حرارتی)، انرژی میدانی (گرانشی، الکترومغناطیسی و هسته ای)، شیمیایی. به طور جداگانه، ارزش آن را دارد که انرژی انفجار را برجسته کنید، ...
انرژی خلاء و هنوز فقط در تئوری موجود است - انرژی تاریک. در این مقاله، اولین مقاله در بخش "مهندسی گرما"، سعی می کنم به زبانی ساده و در دسترس، با استفاده از یک مثال کاربردی، در مورد مهم ترین شکل انرژی در زندگی مردم صحبت کنم - در مورد انرژی حرارتیو در مورد به دنیا آوردن او به موقع قدرت حرارتی.
چند کلمه برای درک جایگاه مهندسی حرارت به عنوان شاخه ای از علم به دست آوردن، انتقال و استفاده از انرژی حرارتی. مهندسی گرما مدرن از ترمودینامیک عمومی بیرون آمده است که به نوبه خود یکی از شاخه های فیزیک است. ترمودینامیک به معنای واقعی کلمه "گرم" به اضافه "قدرت" است. بنابراین، ترمودینامیک علم "تغییر دما" یک سیستم است.
ضربه ای که از بیرون به سیستم وارد می شود، که در آن انرژی داخلی آن تغییر می کند، می تواند نتیجه انتقال حرارت باشد. انرژی حرارتی، که در نتیجه چنین تعاملی با محیط توسط سیستم به دست می آید یا از دست می رود، نامیده می شود مقدار گرماو در سیستم SI بر حسب ژول اندازه گیری می شود.
اگر مهندس گرما نیستید و به طور روزانه با مسائل مهندسی گرما سر و کار ندارید، وقتی با آنها روبرو می شوید، گاهی اوقات بدون تجربه تشخیص سریع آنها می تواند بسیار دشوار باشد. تصور حتی ابعاد مقادیر مورد نظر مقدار حرارت و توان حرارتی بدون تجربه دشوار است. چند ژول انرژی برای گرم کردن 1000 متر مکعب هوا از -37˚C تا +18˚C لازم است؟.. قدرت منبع حرارتی مورد نیاز برای انجام این کار در 1 ساعت چقدر است؟ » نه همه مهندسان. گاهی اوقات متخصصان حتی فرمول ها را به خاطر می آورند، اما فقط تعداد کمی می توانند آنها را عملی کنند!
پس از خواندن این مقاله تا انتها، به راحتی قادر خواهید بود کارهای واقعی تولید و خانگی مربوط به گرمایش و سرمایش مواد مختلف را حل کنید. درک ماهیت فیزیکی فرآیندهای انتقال حرارت و دانش فرمول های ساده پایه بلوک های اصلی در پایه دانش در مهندسی حرارت هستند!
میزان گرما در فرآیندهای فیزیکی مختلف.
بیشتر مواد شناخته شده می توانند در حالت جامد، مایع، گاز یا پلاسما در دماها و فشارهای مختلف باشند. انتقالاز یک حالت کل به حالت دیگر در دمای ثابت صورت می گیرد(به شرط عدم تغییر فشار و سایر پارامترهای محیطی) و با جذب یا آزاد شدن انرژی حرارتی همراه است. علیرغم اینکه 99 درصد ماده در کیهان در حالت پلاسما قرار دارد، ما در این مقاله به این حالت تجمع نخواهیم پرداخت.
نمودار نشان داده شده در شکل را در نظر بگیرید. وابستگی دمای یک ماده را نشان می دهد تیبر میزان گرما سخلاصه شده به یک سیستم بسته خاص حاوی جرم معینی از یک ماده خاص.

1. جامدی که دارای دما است T1، تا یک درجه حرارت گرم می شود Tm، صرف این فرآیند مقداری گرما برابر با Q1 .
2. در مرحله بعد، فرآیند ذوب آغاز می شود که در دمای ثابت رخ می دهد Tpl(نقطه ذوب). برای ذوب کل جرم یک جامد، لازم است انرژی حرارتی را به مقدار مصرف شود Q2 - Q1 .
3. سپس مایع حاصل از ذوب یک جامد تا نقطه جوش (تشکیل گاز) گرم می شود. Tkp، صرف این مقدار گرما برابر با Q3-Q2 .
4. حالا در یک نقطه جوش ثابت Tkpمایع می جوشد و تبخیر می شود و به گاز تبدیل می شود. برای تبدیل کل جرم مایع به گاز، لازم است انرژی حرارتی به مقدار مصرف شود Q4-Q3.
5. در آخرین مرحله، گاز از دما گرم می شود Tkpتا مقداری دما T2. در این صورت هزینه مقدار حرارت خواهد بود Q5-Q4. (اگر گاز را تا دمای یونیزاسیون گرم کنیم، گاز به پلاسما تبدیل می شود.)
بنابراین، جامد اصلی را از دما گرم می کند T1تا دما T2ما انرژی حرارتی را به مقدار مصرف کردیم Q5، ترجمه ماده از طریق سه حالت تجمع.
با حرکت در جهت مخالف، همان مقدار گرما را از ماده خارج می کنیم Q5، عبور از مراحل تراکم، تبلور و سرد شدن از دما T2تا دما T1. البته ما سیستم بسته و بدون تلفات انرژی به محیط خارجی را در نظر داریم.
توجه داشته باشید که انتقال از حالت جامد به حالت گازی با دور زدن فاز مایع امکان پذیر است. این فرآیند تصعید نامیده می شود و فرآیند معکوس آن تصعید نامیده می شود.
بنابراین، ما فهمیدیم که فرآیندهای انتقال بین حالت های کل یک ماده با مصرف انرژی در دمای ثابت مشخص می شود. هنگامی که ماده ای گرم می شود، که در یک حالت تجمع بدون تغییر است، دما افزایش می یابد و انرژی حرارتی نیز مصرف می شود.
فرمول های اصلی انتقال حرارت
فرمول ها بسیار ساده هستند.
مقدار گرما سدر J با فرمول های زیر محاسبه می شود:
1. از سمت مصرف گرما، یعنی از سمت بار:
1.1. هنگام گرم کردن (سرد کردن):
س = متر * ج *(T2 -T1)
متر – جرم ماده بر حسب کیلوگرم
از جانب -ظرفیت گرمایی ویژه یک ماده در J / (kg * K)
1.2. هنگام ذوب (انجماد):
س = متر * λ
λ – گرمای ویژه ذوب و تبلور یک ماده بر حسب J/kg
1.3. در طول جوش، تبخیر (تراکم):
س = متر * r
r – گرمای ویژه تشکیل گاز و تراکم ماده بر حسب J/kg
2. از سمت تولید گرما، یعنی از سمت منبع:
2.1. هنگام سوزاندن سوخت:
س = متر * q
q – گرمای ویژه احتراق سوخت بر حسب J/kg
2.2. هنگام تبدیل برق به انرژی حرارتی (قانون ژول-لنز):
Q =t *I *U =t *R *I ^2=(t /r)*U ^2
تی – زمان در s
من – مقدار فعلی در A
U – ولتاژ r.m.s در V
آر – مقاومت بار بر حسب اهم
نتیجه می گیریم که مقدار گرما به طور مستقیم با جرم ماده در طول تمام تبدیل های فازی متناسب است و هنگامی که گرم می شود، به طور مستقیم با اختلاف دما متناسب است. ضرایب تناسب ( ج , λ , r , q ) برای هر ماده مقادیر خاص خود را دارد و به صورت تجربی تعیین می شود (برگرفته از کتاب های مرجع).
قدرت حرارتی ن در W مقدار حرارتی است که در یک زمان معین به سیستم منتقل می شود:
N=Q/t
هر چه سریعتر بخواهیم بدن را به دمای خاصی گرم کنیم، منبع انرژی حرارتی باید قدرت بیشتری داشته باشد - همه چیز منطقی است.
محاسبه در کار کاربردی اکسل.
در زندگی، اغلب لازم است یک محاسبه تخمینی سریع انجام دهیم تا بفهمیم آیا ادامه مطالعه یک موضوع، ساختن یک پروژه و محاسبات دقیق دقیق و فشرده منطقی است یا خیر. با انجام یک محاسبه در چند دقیقه حتی با دقت 30%، می توانید تصمیم مدیریتی مهمی بگیرید که 100 برابر ارزان تر و 1000 برابر سریعتر و در نتیجه 100000 برابر کارآمدتر از انجام یک محاسبه دقیق در داخل خواهد بود. یک هفته، در غیر این صورت و یک ماه، توسط گروهی از متخصصان گران قیمت ...
شرایط مشکل:
در محل مغازه تهیه نورد فلزی به ابعاد 24 متر در 15 متر در 7 متر از انباری در خیابان به میزان 3 تن نورد وارد می کنیم. فلز نورد دارای یخ با جرم کلی 20 کیلوگرم است. خارج از -37˚С. چه مقدار گرما برای گرم کردن فلز تا + 18 ° C لازم است. یخ را گرم کنید، آن را ذوب کنید و آب را تا +18 درجه سانتیگراد گرم کنید. کل حجم هوای اتاق را گرم کنید، با این فرض که گرمایش قبل از آن کاملاً خاموش شده بود؟ اگر تمام موارد فوق باید در 1 ساعت تکمیل شود، سیستم گرمایش باید چه قدرتی داشته باشد؟ (شرایط بسیار سخت و تقریبا غیر واقعی - به خصوص در مورد هوا!)
محاسبه را در برنامه انجام می دهیمMS Excel یا در برنامهاوو کالک.
برای قالب بندی رنگ سلول ها و فونت ها، صفحه "" را ببینید.
اطلاعات اولیه:
1. نام مواد را می نویسیم:
به سلول D3: فولاد
به سلول E3: یخ
به سلول F3: آب یخ
به سلول G3: اب
به سلول G3: هوا
2. نام فرآیندها را وارد می کنیم:
در سلول های D4، E4، G4، G4: حرارت
به سلول F4: ذوب شدن
3. ظرفیت گرمایی ویژه مواد جدر J / (kg * K) به ترتیب برای فولاد، یخ، آب و هوا می نویسیم
به سلول D5: 460
به سلول E5: 2110
به سلول G5: 4190
به سلول H5: 1005
4. گرمای ویژه همجوشی یخ λ در J/kg وارد کنید
به سلول F6: 330000
5. توده مواد متردر کیلوگرم به ترتیب برای فولاد و یخ وارد می کنیم
به سلول D7: 3000
به سلول E7: 20
از آنجایی که جرم با تبدیل یخ به آب تغییر نمی کند،
در سلول های F7 و G7: =E7 =20
جرم هوا با ضرب حجم اتاق در وزن مخصوص بدست می آید
در سلول H7: =24*15*7*1.23 =3100
6. زمان پردازش تیدر عرض چند دقیقه فقط یک بار برای فولاد می نویسیم
به سلول D8: 60
مقادیر زمانی برای گرم کردن یخ، ذوب شدن آن و گرم کردن آب حاصل از این شرایط محاسبه می شود که همه این سه فرآیند باید در یک زمان با زمان اختصاص داده شده برای گرم کردن فلز جمع شوند. بر این اساس خواندیم
در سلول E8: =E12/(($E$12+$F$12+$G$12)/D8) =9,7
در سلول F8: =F12/(($E$12+$F$12+$G$12)/D8) =41,0
در سلول G8: =G12/(($E$12+$F$12+$G$12)/D8) =9,4
می خوانیم که هوا نیز باید در همان زمان تعیین شده گرم شود
در سلول H8: =D8 =60,0
7. دمای اولیه همه مواد تی1 وارد ˚C می شویم
به سلول D9: -37
به سلول E9: -37
به سلول F9: 0
به سلول G9: 0
به سلول H9: -37
8. دمای نهایی همه مواد تی2 وارد ˚C می شویم
به سلول D10: 18
به سلول E10: 0
به سلول F10: 0
به سلول G10: 18
به سلول H10: 18
فکر می کنم در مورد موارد 7 و 8 نباید هیچ سوالی وجود داشته باشد.

نتایج محاسبات:
9. مقدار گرما سدر KJ مورد نیاز برای هر یک از فرآیندهایی که محاسبه می کنیم
برای گرمایش فولاد در سلول D12: =D7*D5*(D10-D9)/1000 =75900
برای گرم کردن یخ در سلول E12: =E7*E5*(E10-E9)/1000 = 1561
برای ذوب یخ در سلول F12: =F7*F6/1000 = 6600
برای گرم کردن آب در سلول G12: =G7*G5*(G10-G9)/1000 = 1508
برای گرم کردن هوا در سلول H12: =H7*H5*(H10-H9)/1000 = 171330
مقدار کل انرژی حرارتی مورد نیاز برای تمام فرآیندها خوانده می شود
در سلول ادغام شده D13E13F13G13H13: =SUM(D12:H12) = 256900
در سلول های D14، E14، F14، G14، H14، و سلول ترکیبی D15E15F15G15H15، مقدار گرما در واحد اندازه گیری قوس - بر حسب Gcal (بر حسب گیگا کالری) داده می شود.
10. قدرت حرارتی نبر حسب کیلووات، مورد نیاز برای هر یک از فرآیندها محاسبه می شود
برای گرمایش فولاد در سلول D16: =D12/(D8*60) =21,083
برای گرم کردن یخ در سلول E16: =E12/(E8*60) = 2,686
برای ذوب یخ در سلول F16: =F12/(F8*60) = 2,686
برای گرم کردن آب در سلول G16: =G12/(G8*60) = 2,686
برای گرم کردن هوا در سلول H16: =H12/(H8*60) = 47,592
کل توان حرارتی مورد نیاز برای انجام تمام فرآیندها در یک زمان تیمحاسبه شد
در سلول ادغام شده D17E17F17G17H17: =D13/(D8*60) = 71,361
در سلولهای D18، E18، F18، G18، H18 و سلول ترکیبی D19E19F19G19H19، توان حرارتی در واحد اندازهگیری قوس - بر حسب Gcal/h داده میشود.
این محاسبات را در اکسل کامل می کند.
نتیجه گیری:
توجه داشته باشید که برای گرم کردن هوا بیش از دو برابر انرژی لازم برای گرم کردن همان جرم فولاد مصرف می شود.
هنگام گرم کردن آب، هزینه انرژی دو برابر بیشتر از گرم کردن یخ است. فرآیند ذوب چندین برابر بیشتر از فرآیند گرمایش انرژی مصرف می کند (با اختلاف دما کم).
آب گرمایش ده برابر بیشتر از فولاد گرمایشی و چهار برابر بیشتر از هوای گرمایی مصرف می کند.
برای دریافت اطلاعات در مورد انتشار مقالات جدید و برای دانلود فایل های برنامه کاری از شما می خواهم در پنجره ای که در انتهای مقاله یا در بالای صفحه قرار دارد، در اطلاعیه ها مشترک شوید.
پس از وارد کردن آدرس ایمیل خود و کلیک بر روی دکمه "دریافت اطلاعیه های مقاله". فراموش نکنتایید اشتراک، ابونمان با کلیک بر روی لینک در نامه ای که بلافاصله از طریق نامه مشخص شده برای شما ارسال می شود (گاهی اوقات - در پوشه « هرزنامه ها » )!
ما مفاهیم "مقدار گرما" و "قدرت حرارتی" را به یاد آوردیم، فرمول های اساسی برای انتقال حرارت را در نظر گرفتیم و یک مثال عملی را تجزیه و تحلیل کردیم. امیدوارم زبانم ساده، قابل فهم و جالب بوده باشد.
من مشتاقانه منتظر سوالات و نظرات در مورد مقاله هستم!
پرسیدن احترام گذاشتن فایل دانلود اثر نویسنده پس از اشتراک برای اطلاعیه های مقاله
طبق تعریف، کالری مقدار حرارتی است که برای بالا بردن یک سانتیمتر مکعب آب ۱ درجه سانتیگراد لازم است. یک گیگا کالری، که برای اندازه گیری انرژی حرارتی در مهندسی برق حرارتی و تاسیسات استفاده می شود، یک میلیارد کالری است. در 1 متر 100 سانتی متر وجود دارد، بنابراین در یک متر مکعب 100 x 100 x 100 = 1000000 سانتی متر وجود دارد. بنابراین، برای گرم کردن یک مکعب آب توسط
1 درجه، یک میلیون کالری یا 0.001 Gcal نیاز دارد.
در شهر من، قیمت گرمایش 1132.22 روبل / Gcal، و قیمت آب گرم 71.65 روبل / متر مکعب، قیمت آب سرد 16.77 روبل / متر مکعب است.
برای گرم کردن 1 متر مکعب آب چقدر Gcal صرف می شود؟
من هم اینچنین فکر میکنم
s x 1132.22 \u003d 71.65 - 16.77 و به این ترتیب من معادلات را حل می کنم تا بفهمم s (Gcal) برابر با چه چیزی است، یعنی برابر با 0.0484711452 Gcal است.
من به چیزی شک دارم، به نظر من، من اشتباه تصمیم میگیرم
پاسخ:
من هیچ خطایی در محاسبه شما پیدا نمی کنم.
طبیعتاً هزینه فاضلاب (دفع آب) نباید در تعرفه های داده شده لحاظ شود.
یک محاسبه تقریبی برای شهر ایژفسک با توجه به هنجارهای قدیمی به شرح زیر است:
0.19 Gcal برای هر نفر در ماه (این هنجار قبلاً لغو شده است ، اما هیچ چیز دیگری وجود ندارد ، به عنوان مثال انجام خواهد شد) / 3.6 متر مکعب. برای هر نفر در ماه (نرخ مصرف آب گرم) = 0.05278 Gcal در هر 1 متر مکعب. (برای گرم کردن 1 متر مکعب آب سرد تا دمای استاندارد آب گرم که یادآور می شوم 60 درجه سانتیگراد است، حرارت زیادی لازم است).
برای محاسبه دقیق تر مقدار انرژی حرارتی برای گرم کردن آب به روش مستقیم بر اساس مقادیر فیزیکی (و نه برعکس بر اساس تعرفه های مصوب برای تامین آب گرم) - توصیه می کنم از آن استفاده کنید. الگوی محاسبه تعرفه آب گرم (REC UR). فرمول محاسبه، از جمله، از دمای آب سرد در تابستان و زمستان (گرمایش)، مدت زمان این دوره ها استفاده می کند.
برچسب ها: گیگا کالری، آب گرم
- ما هزینه خدمات آب گرم را پرداخت می کنیم، درجه حرارت بسیار کمتر از استاندارد است. چه باید کرد؟
- ادامه دوره قطع اتصال DHW تعیین شده توسط قوانین غیرقانونی نیست - تصمیم دادگاه عالی فدراسیون روسیه (2017)
- ابتکار تعرفه عادلانه تر و روش اندازه گیری آب گرم
- در مورد روش محاسبه مجدد میزان پرداخت گرمایش و تامین آب گرم در هنگام خاموش شدن - شفاف سازی Rospotrebnadzor برای SD
- در مورد حسابداری حامل گرما در یک سیستم تامین حرارت بسته - نامه وزارت ساخت و ساز فدراسیون روسیه 31 مارس 2015 شماره 9116-OD / 04
- UR - در مورد کاهش پرداخت برای تامین آب گرم و گرمایش - نامه وزارت نیرو UR 2015/08/17 شماره 11-10 / 5661
- دوره استاندارد برای بررسی دستگاه اندازه گیری گرمایش و آب گرم خانه مشترک چقدر است؟
- آب داغ کثیف از شیر آب. کجا باید درخواست داد؟
- آیا کنتور آب در آپارتمان می تواند برای کل ورودی منفجر شود؟ نحوه پرداخت؟ نشانه های ماه - 42 متر مکعب
- روش نگهداری جداگانه هزینه ها در زمینه تامین آب و فاضلاب - دستور وزارت ساخت و ساز فدراسیون روسیه مورخ 25 ژانویه 2014 شماره 22 / pr.
- پرداخت آب و برق در آپارتمان بدون مسکن
- محاسبه گرما با توجه به ODPU برای 1/12
- منبع تغذیه
- پرداخت های کلان برای یک اتاق در هاستل (17.3 متر مربع)
| نظرات: (11) | |
| نکته: اگر میخواهید پاسخها/نظرات بیشتری دریافت کنید، پیوند را در رسانههای اجتماعی به اشتراک بگذارید! | |
(یا انتقال حرارت).
ظرفیت گرمایی ویژه یک ماده
ظرفیت گرماییمقدار گرمایی است که بدن با حرارت 1 درجه جذب می کند.
ظرفیت گرمایی بدن با حروف بزرگ لاتین نشان داده می شود از جانب.
چه چیزی ظرفیت گرمایی بدن را تعیین می کند؟ اول از همه، از جرم آن. واضح است که گرم کردن مثلاً 1 کیلوگرم آب نسبت به گرم کردن 200 گرم به حرارت بیشتری نیاز دارد.
در مورد نوع ماده چطور؟ بیایید یک آزمایش انجام دهیم. اجازه دهید دو ظرف یکسان برداریم و با ریختن آب به وزن 400 گرم در یکی از آنها و روغن نباتی به وزن 400 گرم در دیگری، شروع به گرم کردن آنها با کمک مشعل های یکسان می کنیم. با مشاهده قرائت دماسنج ها متوجه می شویم که روغن به سرعت گرم می شود. برای گرم کردن آب و روغن به یک دما، آب باید مدت زمان بیشتری گرم شود. اما هر چه بیشتر آب را گرم کنیم، گرمای بیشتری از مشعل دریافت می کند.
بنابراین، برای گرم کردن یک جرم از مواد مختلف به یک دما، مقادیر متفاوتی گرما مورد نیاز است. مقدار حرارت مورد نیاز برای گرم کردن یک جسم و در نتیجه ظرفیت گرمایی آن بستگی به نوع ماده ای دارد که این جسم از آن تشکیل شده است.
به عنوان مثال، برای افزایش دمای آب با جرم 1 کیلوگرم به میزان 1 درجه سانتیگراد، حرارتی معادل 4200 ژول لازم است و برای گرم کردن همان جرم روغن آفتابگردان به میزان 1 درجه سانتیگراد، مقداری از حرارت برابر با 1700 ژول مورد نیاز است.
کمیت فیزیکی که نشان می دهد چه مقدار گرما برای گرم کردن 1 کیلوگرم یک ماده در 1 ºС نیاز است، نامیده می شود. گرمای ویژهاین ماده
هر ماده ظرفیت گرمایی خاص خود را دارد که با حرف لاتین c نشان داده می شود و بر حسب ژول بر کیلوگرم درجه (J / (kg ° C) اندازه گیری می شود.
ظرفیت گرمایی ویژه یک ماده در حالت های مختلف سنگدانه (جامد، مایع و گاز) متفاوت است. به عنوان مثال، ظرفیت گرمایی ویژه آب 4200 J/(kg ºС) و ظرفیت گرمایی ویژه یخ 2100 J/(kg ºС) است. آلومینیوم در حالت جامد دارای ظرفیت گرمایی ویژه 920 ژول (کیلوگرم - درجه سانتیگراد) و در حالت مایع 1080 ژول / (کیلوگرم - درجه سانتیگراد) است.
توجه داشته باشید که آب ظرفیت گرمایی ویژه بسیار بالایی دارد. بنابراین، آب دریاها و اقیانوس ها که در تابستان گرم می شود، مقدار زیادی گرما را از هوا جذب می کند. به همین دلیل، در مکان هایی که در نزدیکی آب های بزرگ قرار دارند، تابستان به اندازه مکان های دور از آب گرم نیست.
محاسبه مقدار گرمای مورد نیاز برای گرم کردن بدن یا آزاد شده توسط آن در هنگام خنک شدن.
با توجه به مطالب فوق، روشن است که مقدار گرمای لازم برای گرم کردن بدن به نوع ماده ای که بدن از آن تشکیل شده است (یعنی ظرفیت گرمایی ویژه آن) و به جرم بدن بستگی دارد. همچنین مشخص است که میزان گرما بستگی به این دارد که قرار است دمای بدن را چند درجه افزایش دهیم.
بنابراین، برای تعیین مقدار گرمای مورد نیاز برای گرم کردن بدن یا آزاد شده توسط آن در هنگام سرد شدن، باید گرمای ویژه بدن را در جرم آن و در اختلاف دمای نهایی و اولیه آن ضرب کنید:
س = سانتی متر (تی 2 - تی 1 ) ,
جایی که س- مقدار گرما، جظرفیت گرمایی ویژه است، متر- جرم بدن ، تی 1 - دمای اولیه تی 2 دمای نهایی است.
وقتی بدن گرم می شود t 2 > تی 1 و از این رو س > 0 . وقتی بدن خنک شد t 2 و< تی 1 و از این رو س< 0 .
اگر ظرفیت گرمایی کل بدن مشخص باشد از جانب, سبا فرمول تعیین می شود:
Q \u003d C (t 2 - تی 1 ) .
730. چرا از آب برای خنک کردن برخی مکانیسم ها استفاده می شود؟
آب دارای ظرفیت گرمایی ویژه بالایی است که به حذف گرمای خوب از مکانیسم کمک می کند.
731. در چه صورت باید انرژی بیشتری صرف کرد: برای گرم کردن یک لیتر آب در دمای 1 درجه سانتیگراد یا برای گرم کردن صد گرم آب در دمای 1 درجه سانتیگراد؟
برای گرم کردن یک لیتر آب، از آنجایی که جرم بزرگتر است، انرژی بیشتری باید صرف شود.
732. چنگالهای نیکل و نقره به همان جرم را در آب داغ فرو کردند. آیا گرمای یکسانی از آب دریافت می کنند؟
چنگال نیکل نیکل گرمای بیشتری دریافت می کند، زیرا گرمای ویژه کوپرونیکل از نقره بیشتر است.
733. یک تکه سرب و یک قطعه چدن هم جرم با پتک سه ضربه خوردند. کدام قسمت داغتر شد؟
سرب بیشتر گرم می شود زیرا ظرفیت گرمایی ویژه آن کمتر از چدن است و انرژی کمتری برای گرم کردن سرب مورد نیاز است.
734. یک فلاسک حاوی آب و دیگری حاوی نفت سفید با همان جرم و دما است. یک مکعب آهن به همان اندازه گرم شده در هر فلاسک ریخته شد. چه چیزی تا دمای بالاتر گرم می شود - آب یا نفت سفید؟
نفت سفید.
735. چرا نوسانات دما در زمستان و تابستان در شهرهای ساحلی کمتر از شهرهای داخل خشکی است؟
آب کندتر از هوا گرم و سرد می شود. در زمستان سرد می شود و توده های هوای گرم را در خشکی به حرکت در می آورد و آب و هوای ساحل را گرمتر می کند.
736. ظرفیت حرارتی ویژه آلومینیوم 920 ژول بر کیلوگرم درجه سانتیگراد است. این یعنی چی؟
این بدان معناست که برای گرم کردن 1 کیلوگرم آلومینیوم در دمای 1 درجه سانتیگراد 920 ژول نیاز است.
737. میله های آلومینیوم و مس با جرم یک کیلوگرم در دمای 1 درجه سانتیگراد خنک می شوند. انرژی داخلی هر بلوک چقدر تغییر خواهد کرد؟ کدام نوار بیشتر و چقدر تغییر می کند؟
738- برای گرم کردن یک کیلوگرم شمش آهن در دمای 45 درجه سانتی گراد چه مقدار حرارت لازم است؟

739- برای گرم کردن 0.25 کیلوگرم آب از دمای 30 درجه تا 50 درجه سانتیگراد چقدر گرما لازم است؟
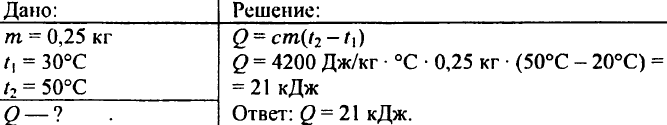
740. انرژی داخلی دو لیتر آب با حرارت 5 درجه سانتی گراد چگونه تغییر می کند؟

741. برای گرم كردن 5 گرم آب از 20 درجه سانتیگراد تا 30 درجه سانتیگراد چه مقدار حرارت لازم است؟
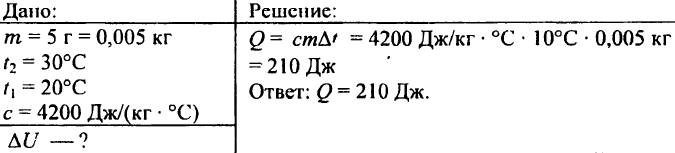
742. برای گرم کردن توپ آلومینیومی به وزن 0.03 کیلوگرم در دمای 72 درجه سانتیگراد چه مقدار گرما لازم است؟
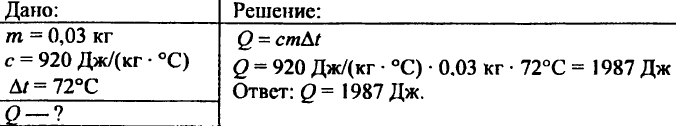
743. مقدار حرارت مورد نیاز برای گرم کردن 15 کیلوگرم مس را در دمای 80 درجه سانتیگراد محاسبه کنید.

744. مقدار حرارت مورد نیاز برای حرارت دادن 5 کیلوگرم مس را از 10 درجه سانتیگراد تا 200 درجه سانتیگراد محاسبه کنید.
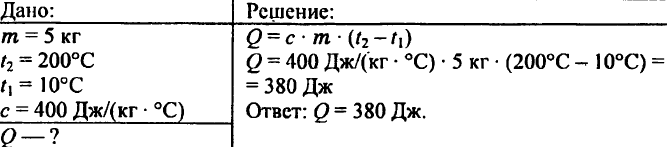
745. برای گرم کردن 0.2 کیلوگرم آب از دمای 15 درجه تا 20 درجه سانتیگراد چه مقدار گرما لازم است؟

746. آب به وزن 0.3 کیلوگرم تا 20 درجه سانتیگراد خنک شده است. انرژی داخلی آب چقدر کاهش می یابد؟

747- برای گرم کردن 0.4 کیلوگرم آب در دمای 20 درجه سانتیگراد تا دمای 30 درجه سانتیگراد چقدر حرارت لازم است؟

748. برای گرم کردن 2.5 کیلوگرم آب در دمای 20 درجه سانتیگراد چقدر گرما صرف می شود؟
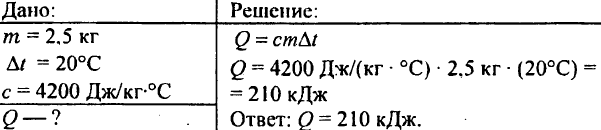
749. وقتی 250 گرم آب از دمای 90 درجه سانتیگراد تا 40 درجه سانتیگراد خنک شد چه مقدار گرما آزاد شد؟
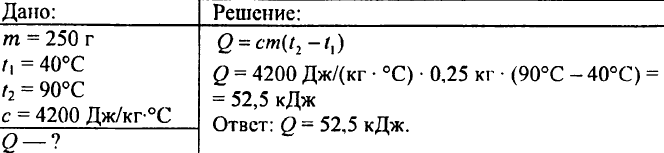
750. برای گرم کردن 0.015 لیتر آب در دمای 1 درجه سانتی گراد چه مقدار گرما لازم است؟

751. مقدار حرارت مورد نیاز برای گرم کردن حوضچه ای با حجم 300 متر مکعب در 10 درجه سانتی گراد را محاسبه کنید؟
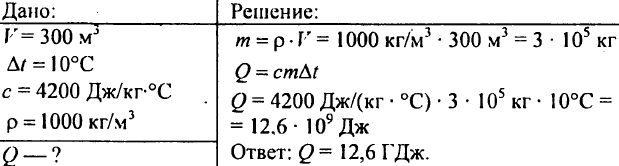
752- چه مقدار حرارت باید به یک کیلوگرم آب داد تا دمای آن از 30 درجه به 40 درجه سانتی گراد برسد؟

753. آب با حجم 10 لیتر از دمای 100 درجه سانتیگراد به دمای 40 درجه سانتیگراد سرد شده است. در این حالت چقدر گرما آزاد می شود؟

754. مقدار حرارت مورد نیاز برای گرم کردن 1 متر مکعب ماسه را در دمای 60 درجه سانتیگراد محاسبه کنید.

755. حجم هوا 60 متر مکعب، ظرفیت حرارتی ویژه 1000 ژول بر کیلوگرم درجه سانتیگراد، چگالی هوا 1.29 کیلوگرم بر متر مکعب. چه مقدار حرارت لازم است تا آن را به 22 درجه سانتیگراد برسانیم؟

756. آب با 10 درجه سانتیگراد گرم شد و 4.20 103 ژول گرما صرف شد. مقدار آب را تعیین کنید.

757. آب با وزن 0.5 کیلوگرم 20.95 کیلوژول گرما گزارش شده است. اگر دمای اولیه آب 20 درجه سانتیگراد بود دمای آب چقدر بود؟

758. 8 کیلوگرم آب در دمای 10 درجه سانتیگراد در قابلمه مسی به وزن 2.5 کیلوگرم ریخته می شود. چقدر حرارت لازم است تا آب در یک قابلمه به جوش بیاید؟

759. یک لیتر آب با دمای 15 درجه سانتیگراد در ملاقه مسی به وزن 300 گرم می ریزند، برای گرم شدن آب ملاقه تا 85 درجه سانتیگراد چقدر حرارت لازم است؟
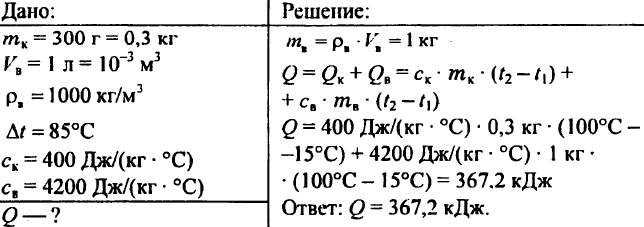
760. یک قطعه گرانیت گرم شده به وزن 3 کیلوگرم در آب قرار می گیرد. گرانیت 12.6 کیلوژول گرما را به آب منتقل می کند و در دمای 10 درجه سانتی گراد خنک می شود. ظرفیت گرمایی ویژه سنگ چقدر است؟

761. آب داغ در دمای 50 درجه سانتی گراد به 5 کیلوگرم آب در دمای 12 درجه سانتی گراد اضافه شد و مخلوطی با دمای 30 درجه سانتی گراد به دست آمد. چقدر آب اضافه شد؟

762. آب در دمای 20 درجه سانتیگراد به 3 لیتر آب در دمای 60 درجه سانتیگراد اضافه شد تا آب در دمای 40 درجه سانتیگراد بدست آید. چقدر آب اضافه شد؟

763. اگر 600 گرم آب در دمای 80 درجه سانتیگراد با 200 گرم آب در دمای 20 درجه سانتیگراد مخلوط شود دمای مخلوط چقدر خواهد بود؟

764. یک لیتر آب 90 درجه سانتیگراد در آب 10 درجه سانتیگراد ریخته شد و دمای آب به 60 درجه رسید. آب سرد چقدر بود؟
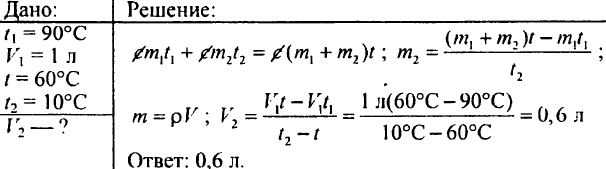
765. تعیین کنید اگر ظرف قبلاً دارای 20 لیتر آب سرد با دمای 15 درجه سانتیگراد باشد چه مقدار آب گرم گرم شده تا 60 درجه سانتیگراد باید در ظرف ریخته شود. دمای مخلوط باید 40 درجه سانتیگراد باشد.
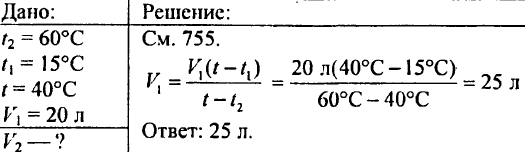
766. تعیین کنید برای گرم کردن 425 گرم آب در دمای 20 درجه سانتیگراد چه مقدار گرما لازم است.

767. اگر آب 167.2 کیلوژول دریافت کند 5 کیلوگرم آب چند درجه گرم می شود؟

768- برای گرم کردن متر گرم آب در دمای t1 تا دمای t2 چقدر گرما لازم است؟
769. 2 کیلوگرم آب در دمای 15 درجه سانتیگراد در گرماسنج ریخته می شود. اگر یک وزن برنجی 500 گرمی که تا 100 درجه سانتیگراد گرم شده باشد، آب گرماسنج تا چه دمایی گرم می شود؟ ظرفیت گرمایی ویژه برنج 0.37 کیلوژول بر (کیلوگرم درجه سانتیگراد) است.

770. تکه های مس و قلع و آلومینیوم هم حجم هست. کدام یک از این قطعات بیشترین و کدام کمترین ظرفیت حرارتی را دارد؟

771. 450 گرم آب که دمای آن 20 درجه سانتیگراد است در کالریمتر ریخته شد. وقتی 200 گرم از براده های آهن که تا دمای 100 درجه سانتی گراد گرم شده بود در این آب غوطه ور شد، دمای آب به 24 درجه سانتی گراد رسید. ظرفیت گرمایی ویژه خاک اره را تعیین کنید.

772. گرماسنج مسی به وزن 100 گرم 738 گرم آب را در خود جای می دهد که دمای آن 15 درجه سانتی گراد است. 200 گرم مس در دمای 100 درجه سانتیگراد به این کالریمتر ریخته شد و پس از آن دمای کالری سنج به 17 درجه سانتیگراد افزایش یافت. ظرفیت حرارتی ویژه مس چقدر است؟

773. یک توپ فولادی به وزن 10 گرم از کوره خارج می شود و در دمای 10 درجه سانتیگراد در آب فرو می رود. دمای آب به 25 درجه سانتیگراد افزایش یافت. اگر جرم آب 50 گرم باشد دمای توپ در فر چقدر بود؟ ظرفیت گرمایی ویژه فولاد 0.5 کیلوژول بر (کیلوگرم درجه سانتیگراد) است.
776. آب به وزن 0.95 گرم در دمای 80 درجه سانتیگراد با آب به وزن 0.15 گرم در دمای 15 درجه سانتیگراد مخلوط شد. دمای مخلوط را تعیین کنید. 779. یک اسکنه فولادی به وزن 2 کیلوگرم تا دمای 800 درجه سانتیگراد گرم شد و سپس در ظرفی حاوی 15 لیتر آب در دمای 10 درجه سانتیگراد فرو رفت. آب ظرف تا چه دمایی گرم می شود؟

(نمایه. برای حل این مشکل باید معادله ای ایجاد کرد که در آن دمای مورد نظر آب در ظرف پس از پایین آمدن کاتر مجهول در نظر گرفته شود.)
780. اگر 0.02 کیلوگرم آب در دمای 15 درجه سانتیگراد، 0.03 کیلوگرم آب در دمای 25 درجه سانتیگراد و 0.01 کیلوگرم آب در دمای 60 درجه سانتیگراد مخلوط شود، آب چه دمایی خواهد داشت؟

781. گرم کردن یک کلاس با تهویه مناسب به مقدار 4.19 مگا ژول در ساعت نیاز دارد. آب در دمای 80 درجه سانتیگراد وارد رادیاتورهای گرمایشی شده و در دمای 72 درجه سانتیگراد از آن خارج می شود. در هر ساعت چقدر آب باید به رادیاتورها برسد؟

782. سرب به وزن 0.1 کیلوگرم در دمای 100 درجه سانتیگراد در گرماسنج آلومینیومی به وزن 0.04 کیلوگرم حاوی 0.24 کیلوگرم آب در دمای 15 درجه سانتیگراد غوطه ور شد. پس از آن دمای 16 درجه سانتیگراد در کالریمتر تعیین شد. ظرفیت گرمایی ویژه سرب چقدر است؟

«...- چقدر طوطی در تو جا می شود، قد تو همین است.
- واقعا لازمه! من این همه طوطی را قورت نمی دهم!…»
از m / f "38 طوطی"
مطابق با قوانین بین المللی SI (سیستم بین المللی واحدها)، مقدار انرژی حرارتی یا مقدار گرما با ژول [J] اندازه گیری می شود، همچنین چندین واحد کیلوژول [kJ] = 1000 J.، MegaJule [MJ] وجود دارد. = 1,000,000 J, GigaJule [ GJ] = 1,000,000,000 J. و غیره این واحد اندازه گیری انرژی حرارتی اصلی ترین واحد بین المللی است و بیشتر در محاسبات علمی و علمی و فنی استفاده می شود.
با این حال، همه ما می دانیم یا حداقل یک بار شنیده ایم که واحد دیگری برای اندازه گیری مقدار گرما (یا فقط گرما) یک کالری است، و همچنین یک کیلو کالری، مگا کالری و گیگا کالری، که به معنای پیشوندهای کیلو، گیگا و مگا است. مثال با ژول بالا. در کشور ما از لحاظ تاریخی توسعه یافته است به طوری که هنگام محاسبه تعرفه های گرمایش، چه گرمایش با برق، چه گاز یا دیگ های گلوله، مرسوم است که هزینه دقیقاً یک گیگا کالری انرژی حرارتی در نظر گرفته شود.
بنابراین گیگا کالری، کیلووات، کیلووات * ساعت یا کیلووات/ساعت و ژول چیست و چه ارتباطی با هم دارند؟، در این مقاله خواهید آموخت.
بنابراین، واحد اصلی انرژی حرارتی، همانطور که قبلا ذکر شد، ژول است. اما قبل از صحبت در مورد واحدهای اندازه گیری، اصولاً لازم است در سطح خانوار توضیح دهیم که انرژی حرارتی چیست و چگونه و چرا آن را اندازه گیری کنیم.
همه ما از دوران کودکی می دانیم که برای گرم کردن (به دست آوردن انرژی حرارتی) باید چیزی را آتش بزنید، بنابراین همه ما آتش روشن می کنیم، سوخت سنتی آتش هیزم است. بنابراین، بدیهی است که در طی احتراق سوخت (هر گونه: هیزم، زغال سنگ، گلوله، گاز طبیعی، سوخت دیزل)، انرژی حرارتی (گرما) آزاد می شود. اما برای گرم کردن مثلاً حجم های مختلف آب، مقدار متفاوتی هیزم (یا سوخت دیگر) لازم است. واضح است که چند آتش در آتش برای گرم کردن دو لیتر آب کافی است و برای پختن نصف سطل سوپ برای کل اردوگاه باید چندین بسته هیزم تهیه کنید. برای اینکه مقادیر فنی سختگیرانه ای مانند مقدار گرما و گرمای احتراق سوخت با بسته های هیزم و سطل سوپ اندازه گیری نشود، مهندسان گرما تصمیم گرفتند تا وضوح و نظم را به ارمغان آورند و موافقت کردند که واحدی برای مقدار گرما اختراع کنند. برای اینکه این واحد در همه جا یکسان باشد، به این صورت تعریف شده است: برای گرم کردن یک کیلوگرم آب در شرایط عادی (فشار اتمسفر) به 4190 کالری یا 4.19 کیلو کالری نیاز است، بنابراین برای گرم کردن یک گرم آب، هزار برابر گرمای کمتر کافی خواهد بود - 4.19 کالری.
کالری مربوط به واحد بین المللی انرژی حرارتی، ژول، به شرح زیر است:
1 کالری = 4.19 ژول.
بنابراین، برای گرم کردن یک گرم آب به اندازه 4.19 ژول انرژی حرارتی و برای گرم کردن یک کیلوگرم آب به 4190 ژول انرژی حرارتی نیاز است.
در فناوری، همراه با واحد اندازه گیری انرژی حرارتی (و هر انرژی دیگر)، یک واحد توان وجود دارد و مطابق با سیستم بین المللی (SI) این واحد وات است. مفهوم قدرت برای وسایل گرمایشی نیز کاربرد دارد. اگر یک دستگاه گرمایشی قادر باشد 1 ژول انرژی حرارتی را در 1 ثانیه تحویل دهد، پس توان آن 1 وات است. قدرت توانایی یک دستگاه برای تولید (ایجاد) مقدار معینی انرژی (در مورد ما، انرژی حرارتی) در واحد زمان است. برگردیم به مثال خودمان در مورد آب، برای گرم کردن یک کیلوگرم (یا یک لیتر، در مورد آب، یک کیلوگرم برابر با یک لیتر) آب یک درجه سانتیگراد (یا کلوین، هر چه باشد)، به توان 1 کیلو کالری نیاز داریم. یا 4190 ژول انرژی حرارتی. برای گرم کردن یک کیلوگرم آب در 1 ثانیه در زمان 1 درجه به دستگاهی با توان زیر نیاز داریم:
4190 J./1 s. = 4 190 وات. یا 4.19 کیلو وات.
اگر بخواهیم در همان ثانیه کیلوگرم آب خود را 25 درجه گرم کنیم، به بیست و پنج برابر بیشتر نیاز داریم، یعنی.
4.19 * 25 \u003d 104.75 کیلو وات.
بنابراین می توان نتیجه گرفت که دیگ پلت با ظرفیت 104.75 کیلو وات. 1 لیتر آب را 25 درجه در یک ثانیه گرم می کند.
از آنجایی که ما به وات و کیلووات رسیدیم، باید در مورد آنها نیز صحبت کنیم. همانطور که گفته شد وات واحدی از توان شامل توان حرارتی دیگ است، اما علاوه بر دیگ های گلوله ای و دیگ های گاز، دیگ های برقی نیز برای بشر آشنا هستند که البته قدرت آن ها در همان کیلووات و نه گلوله مصرف می کنند و نه گاز و برق مصرف می کنند که میزان آن بر حسب کیلووات ساعت اندازه گیری می شود. املای صحیح واحد انرژی کیلووات * ساعت است (یعنی کیلووات ضرب در ساعت، تقسیم نمی شود)، نوشتن کیلووات در ساعت اشتباه است!
در دیگ های برقی انرژی الکتریکی به انرژی حرارتی (به اصطلاح گرمای ژول) تبدیل می شود و اگر دیگ 1 کیلووات ساعت برق مصرف می کرد چقدر گرما تولید می کرد؟ برای پاسخ به این سوال ساده، باید یک محاسبه ساده انجام دهید.
تبدیل کیلووات به کیلوژول/ثانیه (کیلوژول در ثانیه) و ساعت به ثانیه: در یک ساعت 3600 ثانیه وجود دارد، دریافت می کنیم:
1 kW*h =[ 1 kJ/s]*3600 s.=1000 J *3600 s = 3600000 ژول یا 3.6 MJ.
بنابراین،
1 کیلووات ساعت = 3.6 مگاژول.
به نوبه خود 3.6 MJ / 4.19 \u003d 0.859 Mcal \u003d 859 kcal \u003d 859,000 کالری. انرژی (حرارتی).
حالا بیایید به Gigacalorie بپردازیم که قیمت آن برای انواع سوخت مورد علاقه مهندسان حرارت است.
1 Gcal = 1,000,000,000 کالری.
1,000,000,000 کالری \u003d 4.19 * 1,000,000,000 \u003d 4,190,000,000 J. \u003d 4,190 MJ. = 4.19 GJ.
یا با دانستن اینکه 1 کیلووات ساعت = 3.6 مگا ژول، 1 گیگا کالری در هر کیلووات*ساعت را مجددا محاسبه می کنیم:
1 Gcal = 4190 MJ/3.6 MJ = 1163 kWh!
اگر پس از مطالعه این مقاله تصمیم گرفتید در مورد هر موضوعی که مربوط به تامین گرما است با متخصص شرکت ما مشورت کنید، پس شما اینجا!
منبع: heat-en.ru

 نحوه نگهداری قارچ پورسینی پس از برداشت و برای زمستان
نحوه نگهداری قارچ پورسینی پس از برداشت و برای زمستان تنظیم کننده سرعت برای آسیاب - برای اطمینان بیشتر و عملکرد دستگاه
تنظیم کننده سرعت برای آسیاب - برای اطمینان بیشتر و عملکرد دستگاه انتخاب گزینه های استراتژیک
انتخاب گزینه های استراتژیک