Vattnets roll i kroppscellen. Vattnets funktioner i en cell Var finns vatten i en cell
Vattnets egenskaper och dess roll i cellen:
I första hand bland cellens substanser är vatten. Den utgör cirka 80 % av cellens massa. Vatten är dubbelt viktigt för levande organismer, eftersom det är nödvändigt inte bara som en komponent i celler, utan för många också som en livsmiljö.
1. Vatten bestämmer cellens fysiska egenskaper - dess volym, elasticitet.
2. Många kemiska processer sker endast i en vattenlösning.
3. Vatten är ett bra lösningsmedel: många ämnen kommer in i cellen från den yttre miljön i en vattenlösning och i en vattenlösning avlägsnas avfallsprodukter från cellen.
4. Vatten har hög värmekapacitet och värmeledningsförmåga.
5. Vatten har en unik egenskap: när det kyls från +4 till 0 grader expanderar det. Därför visar sig is vara lättare än flytande vatten och ligger kvar på ytan. Detta är mycket viktigt för organismer som lever i vattenmiljön.
6. Vatten kan vara ett bra smörjmedel.
Vattens biologiska roll bestäms av den lilla storleken på dess molekyler, deras polaritet och förmåga att ansluta med varandra genom vätebindningar.
Biologiska funktioner av vatten:
transport. Vatten säkerställer förflyttning av ämnen i cellen och kroppen, absorptionen av ämnen och avlägsnandet av metaboliska produkter. I naturen för vatten avfallsprodukter ut i mark och vatten.
metabolisk. Vatten är mediet för alla biokemiska reaktioner, en elektrondonator under fotosyntesen; det är nödvändigt för hydrolysen av makromolekyler till deras monomerer.
Vatten är inblandat i bildandet av smörjande vätskor och slem, sekret och safter i kroppen.
Med mycket få undantag (ben och tandemalj) är vatten den dominerande komponenten i cellen. Vatten är nödvändigt för cellmetabolism (utbyte), eftersom fysiologiska processer uteslutande sker i en vattenhaltig miljö. Vattenmolekyler är involverade i många enzymatiska reaktioner i cellen. Till exempel sker nedbrytningen av proteiner, kolhydrater och andra ämnen som ett resultat av deras interaktion med vatten som katalyseras av enzymer. Sådana reaktioner kallas hydrolysreaktioner.
Vatten fungerar som en källa till vätejoner under fotosyntesen. Vatten i en cell finns i två former: fritt och bundet. Fritt vatten utgör 95 % av allt vatten i cellen och används huvudsakligen som lösningsmedel och som dispersionsmedium för det kolloidala systemet i protoplasman. Bundet vatten, som bara står för 4% av det totala vattnet i cellen, är löst bundet till proteiner genom vätebindningar.
På grund av den asymmetriska fördelningen av laddningar fungerar vattenmolekylen som en dipol och kan därför bindas av både positivt och negativt laddade proteingrupper. Dipolegenskapen hos en vattenmolekyl förklarar dess förmåga att orientera sig i ett elektriskt fält och fästa vid olika molekyler och sektioner av molekyler som bär en laddning. Som ett resultat bildas hydrater
På grund av sin höga värmekapacitet absorberar vatten värme och förhindrar därigenom plötsliga temperatursvängningar i cellen. Kroppens vatteninnehåll beror på dess ålder och metaboliska aktivitet. Den är högst i embryot (90%) och minskar gradvis med åldern. Vattenhalten i olika vävnader varierar beroende på deras metaboliska aktivitet. Till exempel, i hjärnans grå substans finns det upp till 80% vatten och i benen upp till 20%. Vatten är det viktigaste sättet att flytta ämnen i kroppen (blodflöde, lymfa, stigande och nedåtgående strömmar av lösningar genom växtkärlen) och i cellen. Vatten fungerar som ett "smörjmedel", nödvändigt varhelst det finns gnidningsytor (till exempel i fogar). Vatten har sin maximala densitet vid 4°C. Därför är is, som har en lägre densitet, lättare än vatten och flyter på dess yta, vilket skyddar reservoaren från att frysa. Denna egenskap hos vatten räddar livet på många vattenlevande organismer.
Bokstavligen från barndomen vet varje person att vatten spelar en mycket viktig roll för oss. Hygien, städning, dricka - var och en av dessa integrerade delar av livet är förknippade med vatten. Barnet utforskar världen gradvis och lär sig om vattnets roll i cellen. Kanske, först från detta ögonblick blir det klart hur stor dess betydelse är: livet självt är otänkbart utan vatten. Tack vare dess egenskaper gör det möjligt för komplexa organismer att fungera.
Molekylstruktur
Vattnets roll i en cells liv är direkt relaterad till egenskaperna hos dess struktur. Alla känner till formeln för huvudvätskan i vår kropp. Var och en består av en syreatom och två väteatomer. De kombineras till en enda helhet på grund av polaritet, baserat på bildandet av ett gemensamt elektronpar mellan två atomer. En karakteristisk egenskap hos vattenmolekyler är dess elektriska asymmetri. Syreatomen är mer elektronegativ och drar till sig elektroner från väteatomer starkare. Konsekvensen av detta är en förskjutning av vanliga elektronpar mot syreatomen.
Dipol
Vattnets roll i en cell beror på egenskaperna som är inneboende i detta ämne. Som ett resultat av förskjutningen av ett gemensamt elektronpar blir det polariserat. En vattenmolekyl kännetecknas av närvaron av två poler: varje väteatom har en delvis positiv laddning och varje syreatom har en delvis negativ laddning. Tillsammans skapar de en neutral molekyl.
Således är varje strukturell enhet av vatten en dipol. De strukturella egenskaperna hos molekylen bestämmer också karaktären på sambandet mellan angränsande strukturer. Den delvis negativa syreatomen attraheras till väteatomerna i andra molekyler. Mellan dem bildas så kallade vätebindningar. Varje vattenmolekyl strävar efter att kommunicera på liknande sätt med sina fyra grannar. Alla dessa strukturella nyanser bestämmer vattnets biologiska roll i cellen.

Egenheter
Vätebindningar, karakteristiska för vattenmolekyler, bestämmer många av dess egenskaper. Kopplingarna mellan syre- och väteatomer är särskilt starka, vilket innebär att bryta dem kräver en imponerande mängd energi. Som ett resultat har vatten en hög kokpunkt, såväl som smältning och förångning. Bland liknande ämnen är vatten det enda ämne som finns på jorden samtidigt i tre aggregationstillstånd. Vattnets roll i en cell är också baserad på denna egenskap.

Interaktion med hydrofila ämnen
Vattenpartiklarnas inneboende förmåga att bilda vätebindningar gör att huvudkroppsvätskan kan lösa upp många föreningar. Sådana ämnen kallas hydrofila, det vill säga "vänliga" mot vatten. Dessa inkluderar joniska föreningar: salter, baser och syror. Hydrofila ämnen inkluderar även nonjoniska föreningar som har polaritet. Deras molekyler innehåller laddade grupper. Dessa är aminosyror, sockerarter, enkla alkoholer och några andra föreningar.
Vattnets roll i en cells liv reduceras till att skapa den miljö som är nödvändig för att påskynda alla reaktioner. En lösning är ett tillstånd av ett ämne där alla dess molekyler kan röra sig mycket mer fritt, det vill säga att förmågan att reagera blir mycket högre än i sin vanliga form.
Tack vare dessa egenskaper har vatten blivit det huvudsakliga mediet för de allra flesta kemiska reaktioner. Dessutom utförs till exempel hydrolys och hela uppsättningen redoxprocesser endast med direkt deltagande av huvudcellsvätskan.
Reagens
Vattnets enorma roll i en cells liv är obestridlig. Hon deltar i alla viktiga processer. Till exempel är vatten nödvändigt för fotosyntesen. Ett av dess stadier, fotolys av vatten, innebär separation av väteatomer och deras inkludering i de resulterande organiska föreningarna. I detta fall släpps frigjort syre ut i atmosfären.

Människor och djur är förknippade med den redan nämnda hydrolysen, förstörelsen av ämnen med tillsats av vatten. En av de viktigaste reaktionerna av detta slag i en cell är nedbrytningen av ATP-molekylen, som sker med frigörandet av energi, som används för andra livsviktiga processer.
Interaktion med hydrofoba ämnen
Vissa proteiner, liksom fetter och nukleinsyror, löses inte alls i vatten, eller så är denna process mycket svår. Sådana ämnen kallas hydrofoba, det vill säga "rädsla" för vatten. Vattnets roll i cellen och kroppen är också förknippad med dess interaktion med liknande föreningar.
Vattenmolekyler kan separera från själva vätskan. Som ett resultat bildas så kallade gränssnitt. Många kemiska reaktioner äger rum på dem. Det är alltså tack vare interaktionen mellan fosfolipiderna som utgör cellmembranet med vatten som ett lipiddubbelskikt bildas.
Värmekapacitet
I cellen ligger i dess deltagande i termoreglering. ganska hög. Det betyder att när en imponerande mängd absorberas ändras vattnets temperatur endast något. Denna egenskap hjälper till att upprätthålla en konstant temperatur inuti cellen, vilket är nödvändigt för den normala förekomsten av många processer och för att upprätthålla en konstant inre miljö.
Jämn värmefördelning
En annan karakteristisk egenskap hos vatten är värmeledningsförmåga. Det hjälper också till att upprätthålla en konstant inre miljö. Vatten kan överföra en imponerande mängd värme från ett område av kroppen där det är i överskott till de celler och vävnader som saknar det.
Dessutom utförs termoreglering också på grund av det faktum att under övergången från ett aggregationstillstånd till ett annat måste vätebindningar förstöras. Och detta kräver, som redan nämnts, stora mängder energi.
Hydrostatiskt skelett
Vattnets roll i en cells liv slutar inte där. Huvudkroppsvätskan har en annan egenskap: den komprimeras praktiskt taget inte. Denna egenskap tillåter vatten att spela rollen som ett hydrostatiskt skelett i cellen. Vatten skapar turgortryck och bestämmer därigenom egenskaper hos celler och vävnader som volym och elasticitet. Det är lätt att förstå vattnets roll i en cell i denna mening om man tittar på träd. Den vanliga bladformen skapas på grund av ökat tryck i cellerna. Det finns många liknande exempel i den ekologiska världen. Till exempel stöds den välbekanta formen av maneter eller rundmaskar också av ett hydrostatiskt skelett.

Förlust av vatten från celler leder följaktligen till omvända processer. En förändring i form börjar: bladen vissnar, frukterna skrynklas, huden förlorar sin elasticitet.
Deltagande i transport av ämnen
Vattenmolekyler, med hjälp av vätebindningar, kan ansluta inte bara till varandra utan också med andra ämnen. Som ett resultat av denna interaktion uppstår ett ämne som spelar en betydande roll i transporten av ämnen i kroppen. Således är en konsekvens av sammanhållning (vidhäftning av molekyler under påverkan och, i fallet med vatten, genom vätebindningar) rörelsen av näringsämnen i växternas kapillärer. Tack vare samma egenskap rör sig vatten från jorden genom rothåren in i växten.
Ytspänningskraften gör också att kapillärt blodflöde möjliggörs hos djur och människor. Vatten är involverat i förflyttning av ämnen och avlägsnande av sönderfallsprodukter från kroppen.

Det visar sig att svaret på frågan "vad är vattnets roll i cellen?" ganska entydigt - det är enormt. Tack vare de grundläggande egenskaperna hos denna vätskas molekylära struktur är alla grundläggande processer möjliga, utan vilka livet är otänkbart. Vatten hjälper till att öka ämnens reaktivitet, bibehåller formen på celler och organ, deltar i att förse dem med allt de behöver och är en del av många kemiska reaktioner. Vatten är källan till liv och detta är definitivt inte en metafor. Alla större metaboliska processer är förknippade med det, och det ligger också bakom interaktionen mellan olika föreningar.

Det är på grund av dessa egenskaper som vatten är det ämne som man söker först när man utforskar andra planeter i ett försök att förstå om de är lämpliga för liv.
Vissa elever måste skriva en uppsats i skolan om ämnet: "Vilken roll spelar vatten i en cell?" Och varje flitig student från en allmän biologikurs vet att utan den är mänsklighetens liv omöjligt. Om en person förlorar upp till 3% av vätskan börjar han känna sig törstig. Med en förlust på cirka 20 % av vätskan börjar celler i en levande organism dö, vilket i slutändan leder till döden.
I kontakt med
Klasskamrater
Vattnets betydelse för celllivet
På vår planet är detta ämne den vanligaste. Varje cell i en levande organism innehåller mer av det, desto mer intensivt deltar den i metaboliska processer.
Detta ämne finns i kroppen i både bundna och fria former. Fri vätska är involverad i transporten från den yttre miljön till cellen och vice versa. Den fria vätskan fungerar som ett lösningsmedel och ingår i en mängd av 95 % av den totala massan. Det finns i organhålor, vakuoler, intercellulärt utrymme och blodkärl.
Bunden vätska kan hittas mellan fibrer, proteinmolekyler, membran, i cellulära strukturer och bildar föreningar med vissa proteiner. Bunden vätska i varje cell innehåller inte mer än 4% av det totala.
Egenskaper
Detta ämne är viktigare för människor, som alla andra levande organismer, än mat. . Det är huvudelementet i kroppens liv och ger:

Som en del av vilken cell som helst, som kan ses i tabellen nedan, vatten tar första plats vad gäller kvantitativ sammansättning.
Funktioner
Som du vet från skolkemikurser fungerar vatten som en katalysator för olika processer i kroppen. Olika kemiska reaktioner inträffar inuti cellerna i någon levande organism, där vatten deltar som en reaktant.
Under matsmältningsprocessen uppstår proteiner, kolhydrater och fetter med deltagande av vattenmolekyler och energi frigörs som kan stödja vitala processer.
Deltagande i hydrolysen av salter gör att det kan fungera som en källa för protoner och elektroner. Huvudindikatorn för intracellulära processer är förmågan hos en flytande substans att delta i reversibel jonisering och bilda bindningar med väte.
Transportfunktion Detta ämne utför också funktioner inuti organen i en levande organism. Alla avfallsprodukter från cellen utsöndras av flytande molekyler. Näringsämnen levereras till cellerna av molekyler av ett flytande ämne, som tränger in i det intercellulära utrymmet.
Huvudkomponenten för lymf och blod är flytande. Dess brist i kroppen leder till förtjockning av blodet och sköra blodkärl. Lokalt uttrycks detta i form av trombos och blödning.
Konstansen i strukturen av organ och vävnader säkerställs av det faktum att den inte komprimeras i flytande form, bildar optimalt intracellulärt tryck och upprätthåller cellens struktur.
En konstant temperatur inne i kroppen upprätthålls på grund av att vätskemolekylen är värmeintensiv struktur. En stor mängd energi genereras också vid nedbrytningen av fetter, vilket också tjänar till att hålla optimal temperatur.
Detta ämne har en liten molekylstorlek, polaritet och förmågan hos molekyler att ansluta med varandra med hjälp av vätebindningar, vilket bestämmer dess biologiska roll.
Vatten har två funktioner: ur synvinkel av biologiska processer:

Fotolys
Under fotosyntesen detta ämne är en källa till vätejoner. Fotolys sker under fotosyntesen. Översatt från grekiska betyder detta fenomen upplösning, sönderfall eller sönderdelning med ljusets deltagande. Fotolys sker under fotosyntesens lätta fas, där molekylen av detta ämne under påverkan av ljus bryts ner till joner.
Fotolys bryter ner en vattenmolekyl till protoner och elektroner och frigör syre som en biprodukt. Det är detta syre som alla levande varelser på planeten andas.





Vatten är den vanligaste föreningen i levande system. Men vattenhalten varierar kraftigt: från 10% (tandemalj), 20% (benvävnad), till 85% (mänsklig hjärna), i torra frön 10-12%, hos maneter 95-98%, d.v.s. hela kroppen är i huvudsak gjord av vatten. Förlust av 20 % vatten leder till celldöd eller avstängd animering.
Vattnets egenskaper är unika, d.v.s. ingen annan förening har dem. Detta beror på strukturen av dess molekyler: en syreatom är ansluten med en stark kovalent bindning till två väteatomer, d.v.s. H 2 O är en mycket enkel förening. Väteatomer är bundna till syre i en vinkel på 104,5 0.
Figur 1. Strukturen av en vattenmolekyl.
Funktionerna hos vattens fysikaliska egenskaper är förknippade med strukturen hos dess molekyl och egenskaperna hos intermolekylära interaktioner. Fördelningen av elektrontäthet i en vattenmolekyl är sådan (fig. 1, b, c) att 4 poler av laddningar skapas: 2 positiva, associerade med väteatomer, och 2 negativa, associerade med elektronmolnen av elektroner i syret atom. De angivna 4 laddningspolerna är belägna vid tetraederns hörn (fig. 1, d). På grund av detta är vattenmolekylen dipol, och de fyra laddningspolerna tillåter varje molekyl att bilda fyra vätebindningar med närliggande (samma) molekyler. Som ett resultat bildas kluster (när de är omedelbart frysta ser de ut som vackra snöflingor, fig. 2.).


Fig.2. Bildandet av ett vattenkluster.
Kluster bildas arbetssätt "vattenstruktur". Vätebindningar är svaga, 15-20 gånger svagare än kovalenta bindningar. Därför bryts vissa kopplingar lätt, medan andra uppstår. Som ett resultat är molekylerna mycket rörliga. Eventuella yttre förändringar (temperatur, tryck, etc.) förändrar denna arbetsstruktur. Sålunda har vatten hög känslighet och minne.
Vattenmolekyler kan fästa vid molekyler som bär en elektronisk laddning, vilket resulterar i bildandet av hydrater. Om attraktionskraften mellan vattenmolekyler är mindre än vattnets attraktion till ett ämnes molekyler löser sig ämnet.
Vattnets egenskaper och funktioner.
1. Förbinder all levande och livlös natur på planeten till ett enda system. Vatten är rörligt och föränderligt, men det är inte den kemiska sammansättningen av molekylerna som förändras, utan klustrets struktur.
2. Vatten är ett universellt lösningsmedel. På grund av sin polaritet har den ingen motsvarighet i detta: fler ämnen löser sig i vatten än i några andra vätskor. Ämnen kommer in och ut ur cellen endast i upplöst form.
3. I förhållande till vatten delas ämnen i cellen in i 2 grupper:
a) hydrofob (fobos - rädsla, skräck): olöslig i vatten (fetter, polysackarider, etc.)
b) hydrofil (fileon – kärlek): löslig i vatten (mineralsalter, syror, monosackarider, etc.)
På grund av denna egenskap hos vatten (på grund av hydrofoba interaktioner) samlas följande i cellen:
1) biologiska membran,
2) proteiner och DNA tar formen av en spiral.
4. Vatten kännetecknas av hög värmekapacitet (d.v.s. det krävs mycket energi för att höja temperaturen på vattnet och bryta vätebindningar). Så kokpunkten för vatten är 100 0 C, och den för alkohol är 70 0 C.
5. Hög värmeledningsförmåga. Tack vare denna egenskap upprätthålls termisk jämvikt i cellen och kroppen.
6. Vatten självt, som en kemisk förening, deltar i många kemiska reaktioner. Till exempel inträffar hydrolysreaktioner på grund av tillsats av vatten.
7. Det är en källa till O 2 och H + under fotosyntes (fotolys av vatten).
8. Vatten är det huvudsakliga mediet för transport av ämnen i cellen (diffusion) och kroppen (blod- och lymfflöden, interstitiell vätska innehållande näringsämnen, O 2 och CO 2, hormoner, ämnen som tänder och stänger av gener). Detta är en transportfunktion.
9. Ger cellvolym och elasticitet: turgor och osmotiskt tryck, bibehåller formen på celler och organismer (hydroskelett i runda och annelids).
10. Gödslingsmedium.
11. Miljö för vattenlevande organismers liv.
12. Medium för utveckling av djurembryon (i amnion).
13. Deltar i bildandet av smörjvätskor i leder, pleurahålan och perikardsäcken.
14. Bildar slem, vilket säkerställer förflyttning av ämnen genom tarmarna, en fuktig miljö på slemhinnorna (nysningar, hosta).
15. Deltar i bildandet av sekret (saliv, tårar, galla, spermier och salter i kroppen).
16. Vatten är den begränsande faktorn för liv på vår planet. Varhelst det finns vatten, finns det liv, varhelst det inte finns vatten, finns det inget liv.
Vatten är ett unikt ämne. Det är distribuerat överallt på vår planet. Försök föreställa dig hur vårt liv skulle se ut utan H2O-molekylen? Och det finns inget att föreställa sig - det skulle inte finnas något liv på vår planet. Människor är 70% vatten. Ju yngre kroppen är, desto mer innehåller den, och med åldern minskar denna mängd. Låt oss till exempel ta ett embryo - andelen H2O i det är 90%.
I artikeln inbjuder vi dig att markera allt i cellen och överväga var och en i detalj. Det är viktigt att nämna att den finns där i två former: fri och bunden. Vi kommer att ta itu med detta lite senare.
Vatten
Alla vet att vatten spelar en mycket viktig, eller snarare, en nyckelroll i våra liv. Utan den skulle vår planet vara en död, livlös öken. Forskare studerar fortfarande vatten och dess roll i människokroppen.
Vi har redan sagt att vatten finns i våra celler i fria och bundna former. Den första tjänar till att distribuera ämnen - att överföra dem in i och ut ur cellen. Och den sista observeras:
- mellan fibrer;
- membran;
- proteinmolekyler;
- cellulära strukturer.
Både fritt och bundet vatten i cellen utför nödvändigtvis vissa funktioner, som vi kommer att prata om senare. Och nu några ord om hur själva H2O-molekylen är organiserad.
Molekyl
Till att börja med, låt oss beteckna molekylformeln för vatten: H2O. Detta är ett mycket vanligt ämne på planeten, och du bör komma ihåg det, eftersom molekylformeln för vatten finns ganska ofta inom olika kunskapsområden. Förresten, det finns i alla mänskliga organ, även i tandemalj och ben, även om dess andel där är mycket liten - 10% respektive 20%.

Som vi redan har sagt, ju yngre kroppen är, desto mer vatten innehåller den. Forskare har föreslagit att vi åldras eftersom protein inte kan binda stora mängder vatten. Men detta är dock bara en hypotes.
Funktioner
Låt oss nu markera fler av dem tydligt från listan nedan:
- H2O kan fungera som lösningsmedel, eftersom nästan alla kemiska reaktioner är joniska och sker i vatten. Det bör noteras att det finns hydrofila ämnen (som löser till exempel alkohol, socker, aminosyror och så vidare), men det finns också hydrofoba (fettsyror, cellulosa och andra).
- Vatten kan fungera som ett reagens.
- Utför transport-, termoreglerande och strukturella funktioner.
Vi föreslår att vi överväger var och en av dem separat. Låt oss gå i ordning, den första på vår lista är lösningsmedelsfunktionen.
Lösningsmedel
Vattnets funktioner i cellen är många, men en av de viktigaste är att hjälpa till att underlätta många reaktioner. H2O-molekylen kan fungera som ett lösningsmedel. Nästan alla reaktioner som förekommer i en cell är joniska, det vill säga mediet där de kan ske är vatten.
Reagens

Nästa funktioner för vatten i en cell är dess deltagande i kemiska reaktioner som äger rum i kroppen som ett reagens. Dessa inkluderar:
- hydrolys;
- polymerisation;
- fotosyntes och så vidare.
Nu lite om det inom kemi är detta namnet på ett ämne som deltar i vissa kemiska reaktioner. Det viktigaste är att även om det deltar i reaktionen är det inte föremål för bearbetning. Reagenser i laboratoriet (även kallade reagenser) är ett ganska vanligt fenomen.
Vatten, som ett reagens, är involverat i sammansättningen av andra ämnen som kroppen behöver.
Transportfunktion
Varför lever vi? Vår kropp existerar bara för att cellerna som den består av är levande. Och de borde tacka sin unika struktur och några av H2O-molekylens förmågor. Vi har redan nämnt att vatten är en integrerad del av vår kropp, och varje cell innehåller dessa unika molekyler, eller snarare, är i första hand i sin sammansättning.
Vattnets transportfunktion i cellen är ett annat syfte med H2O i vår kropp. Vatten har en viss egenskap - penetration in i det intercellulära utrymmet, tack vare vilka näringsämnen kommer in i cellen.
Det är också värt att veta att blod och lymfa också innehåller vatten, och dess brist leder till några konsekvenser: blödningar eller tromboser.
Termoreglering

Vilka funktioner av vatten i en cell har vi ännu inte räknat ut? Naturligtvis termoreglering. Vi sa att vatten kan absorbera värme och hålla kvar den under lång tid. Således kan H2O skydda cellen från hypotermi eller överhettning. Funktionen av termoreglering behövs inte bara för enskilda celler, utan också för hela organismen som helhet.
Strukturell funktion
Vi har redan listat det, men ytterligare ett syfte återstår att diskutera - att upprätthålla cellstrukturen.
Har du någonsin försökt att komprimera flytande vatten? Även i laboratorieförhållanden är detta extremt svårt att uppnå. Denna egenskap hos vatten är nödvändig för att bibehålla formen och strukturen hos varje cell.
Kom ihåg för alltid: utan vatten är livet omöjligt. Vi upplever törst när kroppen förlorar cirka 3 % vatten, och med en förlust på 20 % dör cellerna, och följaktligen även personen. Se hur mycket vatten du dricker.
 Egenskaper för numeriska funktioner Kontrollera läxor
Egenskaper för numeriska funktioner Kontrollera läxor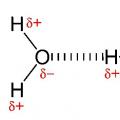 Vattnets funktioner i en cell Var finns vatten i en cell
Vattnets funktioner i en cell Var finns vatten i en cell Afrikas allmänna ekonomiska och geografiska särdrag
Afrikas allmänna ekonomiska och geografiska särdrag