کار آزمایشی: نظریه احتراق و انفجار. تئوری احتراق مخلوط های گاز. فشار انفجار میزان افزایش فشار انفجار
مطالعه فرآیندهای احتراق مخلوط های قابل احتراق توسط دانشمندان روسی و خارجی امکان اثبات نظری بسیاری از پدیده های همراه با فرآیند احتراق از جمله سرعت انتشار شعله را فراهم کرد. مطالعه سرعت انتشار شعله در مخلوط های گازی امکان تعیین سرعت مطمئنه جریانهای گاز-هوا در تهویه ، احیا ، خطوط لوله آسپیراسیون و در خطوط لوله سایر تاسیسات را دارد ، که از طریق آنها مخلوط های گاز و گرد و غبار هوا حمل می شود.
در سال 1889 ، دانشمند روسی V.A. میکلسون دو مورد محدود انتشار شعله را در هنگام احتراق نرمال یا کند و در هنگام انفجار در نظر گرفت.
نظریه انتشار و انفجار طبیعی شعله بیشتر در آثار N.N. سمنوا ، ک.ی. Shchelkina ، D.A. Frank-Kamenetsky ، L.N. Khitrina ، A.S. Sokolik ، V.I. اسكوبلكین و سایر دانشمندان ، و همچنین دانشمندان خارجی B. Lewis ، G. Elbe و دیگران. در نتیجه ، نظریه اشتعال مخلوط های منفجره ایجاد شد. با این حال ، تلاش برای تفسیر پدیده های انتشار شعله به عنوان انتشار مراکز فعال یا توضیح حدود انتشار شعله توسط شرایط شکست زنجیره ، به اندازه کافی قانع کننده نیست.
در سال 1942 ، دانشمند شوروی Ya.B. زلدوویچ مفاد تئوری احتراق و انفجار گازها را فرموله کرد. تئوری احتراق به سالات اصلی پاسخ می دهد: آیا مخلوطی از یک ترکیب معین قابل اشتعال است ، میزان سوختن یک مخلوط انفجاری چقدر خواهد بود ، چه ویژگی ها و اشکال شعله را باید انتظار داشت. این تئوری می گوید که انفجار مخلوط گاز یا بخار هوا یک پدیده فوری نیست. هنگامی که منبع جرقه زنی به مخلوط قابل احتراق وارد می شود ، واکنش اکسیداسیون سوخت با اکسید کننده در ناحیه منبع احتراق آغاز می شود. سرعت واکنش اکسیداسیون در برخی از حجم اولیه این منطقه به حداکثر می رسد - احتراق رخ می دهد. احتراق در مرز حجم اولیه با محیط را شعله جلویی می نامند. جلوی شعله مانند یک کره است. ضخامت جلوی شعله ، محاسبه شده توسط Ya.B. Zeldovich ، برابر است با 1 - 100 میکرون. اگرچه ضخامت ناحیه احتراق کم است ، اما برای ادامه واکنش احتراق کافی است. دمای جلوی شعله به دلیل گرمای واکنش احتراق 1000 - 3000 0 С است و به ترکیب مخلوط قابل احتراق بستگی دارد. دمای مخلوط نیز نزدیک جبهه شعله افزایش می یابد ، که به دلیل انتقال گرما توسط هدایت حرارتی ، انتشار مولکول های گرم شده و تابش است. در سطح خارجی قسمت جلوی شعله ، این دما برابر با دمای خود احتراق مخلوط قابل احتراق است. تغییر دمای مخلوط در امتداد محور لوله در لحظه های زمان به صورت گرافیکی در شکل نشان داده شده است. 4.1 لایه گاز QC 1، که در آن دمای مخلوط افزایش می یابد ، قسمت جلوی شعله است. با افزایش دما ، قسمت جلوی شعله منبسط می شود (تا QC 2) به طرف دیواره های انتهایی لوله ولیو م، مخلوط نسوخته را با سرعت کمی به سمت دیوار جابجا می کند م، و گاز سوخته به سمت دیوار است ولی... بعد از احتراق مخلوط قابل احتراق ، شکل کروی شعله خیلی سریع تحریف شده و بیشتر و بیشتر به سمت مخلوطی که هنوز مشتعل نشده کشیده می شود. کشش جلوی شعله و افزایش سریع سطح آن با افزایش سرعت حرکت همراه است
قسمت مرکزی شعله. این شتاب تا زمانی که شعله به دیواره های لوله ها نرسد یا در هر صورت به دیواره لوله نزدیک شود ادامه دارد. در این لحظه ، اندازه شعله به شدت کاهش می یابد و فقط قسمت کوچکی از شعله باقی می ماند و کل قسمت لوله را می پوشاند. کشش قسمت جلوی شعله و شتاب شدید آن بلافاصله پس از اشتعال توسط جرقه ، زمانی که شعله هنوز به دیواره های لوله نرسیده است ، در اثر افزایش حجم محصولات احتراق ایجاد می شود. بنابراین ، در مرحله اولیه روند تشکیل جبهه شعله ، بدون در نظر گرفتن میزان قابل احتراق مخلوط گاز ، شتاب و کاهش سرعت بعدی شعله اتفاق می افتد و این کاهش سرعت بیشتر خواهد بود ، سرعت شعله بیشتر خواهد بود.

برنج. 4.1 تغییر دما در جلو و پشت شعله شعله: 1 - منطقه
محصولات احتراق 2 - شعله جلو 3 - منطقه خود اشتعال ؛
4 - منطقه پیش گرم 5 - مخلوط اولیه
توسعه مراحل بعدی احتراق تحت تأثیر طول لوله است. کشیدگی لوله منجر به ظهور ارتعاشات و تشکیل ساختار سلولی شعله ، شوک و انفجار امواج می شود.
عرض منطقه گرمایش را جلوتر از جلوی شعله در نظر بگیرید. در این منطقه هیچگونه واکنش شیمیایی اتفاق نمی افتد و گرما تولید نمی شود. عرض منطقه گرمایش من(در سانتی متر) از وابستگی می توان تعیین کرد:
جایی که ولی- ضریب نفوذ حرارتی ؛ v- سرعت انتشار شعله.
برای یک مخلوط متان و هوا ، عرض منطقه گرمایی 0.0006 متر است ، برای مخلوط هیدروژن و هوا بسیار کوچکتر است (3 میکرون). احتراق بعدی در مخلوطی اتفاق می افتد که حالت آن قبلاً در نتیجه رسانایی گرمایی و انتشار اجزا از لایه های مجاور تغییر کرده است. مخلوط کردن محصولات واکنش تأثیر کاتالیزوری خاصی روی سرعت حرکت شعله ندارد.
حال اجازه دهید سرعت حرکت جلوی شعله را از طریق مخلوط گاز در نظر بگیریم. سرعت حرکت خطی v(در متر بر ثانیه) را می توان با فرمول تعیین کرد
سرعت احتراق جرم کجا است ، g / (cm × m 2) ، p تراکم مخلوط احتراق اولیه ، کیلوگرم در متر مکعب است.
سرعت خطی قسمت جلوی شعله ثابت نیست ، این بسته به ترکیب مخلوط و ترکیب گازهای بی اثر (غیر قابل احتراق) ، دمای مخلوط ، قطر لوله ها و غیره تغییر می کند. حداکثر سرعت انتشار شعله نه در غلظت استوکیومتری مخلوط ، بلکه در مخلوط با سوخت اضافی مشاهده می شود. وقتی گازهای بی اثر به مخلوط قابل احتراق وارد می شوند ، سرعت انتشار شعله کاهش می یابد. این امر با کاهش دمای احتراق مخلوط توضیح داده می شود ، زیرا بخشی از گرما صرف گرم کردن ناخالصی های بی اثر می شود که در واکنش شرکت نمی کنند. سرعت انتشار شعله تحت تأثیر ظرفیت حرارتی گاز بی اثر است. هرچه ظرفیت حرارتی گاز بی اثر بیشتر باشد ، دمای احتراق را کاهش می دهد و سرعت انتشار شعله را بیشتر می کند. بنابراین ، در مخلوط متان با هوای رقیق شده با دی اکسید کربن ، سرعت انتشار شعله تقریباً سه برابر کمتر از مخلوطی است که با آرگون رقیق شده است.
هنگامی که مخلوط از قبل گرم می شود ، سرعت انتشار شعله افزایش می یابد. مشخص شد که سرعت انتشار شعله متناسب با مربع دمای اولیه مخلوط است.
با افزایش قطر لوله ها ، سرعت انتشار شعله به طور ناموزونی افزایش می یابد.
با افزایش قطر لوله ها به 0.10 - 0.15 متر ، سرعت خیلی سریع رشد می کند. با افزایش بیشتر قطر لوله ها ، همچنان افزایش می یابد ، اما به میزان کمتری. افزایش دما تا زمانی اتفاق می افتد که قطر به یک قطر محدود کننده خاص برسد ، که بالاتر از آن افزایش سرعت اتفاق نمی افتد. با کاهش قطر لوله ، سرعت انتشار شعله کاهش می یابد و در یک قطر کوچک خاص ، شعله در لوله گسترش نمی یابد. این پدیده را می توان با افزایش تلفات گرما از طریق دیواره های لوله توضیح داد.
بنابراین ، برای جلوگیری از انتشار شعله در مخلوط قابل احتراق ، لازم است که دمای مخلوط را به یک روش یا دیگری کاهش دهید ، با خنک کردن ظرف (در مثال ما یک لوله) از خارج یا با رقیق کردن مخلوط با یک گاز بی اثر سرد.
سرعت نرمال انتشار شعله نسبتاً کم است (بیش از ده متر در ثانیه) ، اما تحت برخی شرایط ، شعله در لوله ها با سرعت فوق العاده (از 2 تا 5 کیلومتر در ثانیه) گسترش می یابد ، بیش از سرعت صدا در یک محیط معین این پدیده را انفجار نامیدند. ویژگی های متمایز انفجار به شرح زیر است:
1) نرخ سوختن ثابت بدون توجه به قطر لوله ؛
2) فشار شعله بالا ناشی از موج انفجار ، که می تواند بیش از 50 مگاپاسکال باشد ، بسته به ماهیت شیمیایی مخلوط قابل احتراق و فشار اولیه ؛ علاوه بر این ، به دلیل سرعت بالا در سوزاندن ، فشار ایجاد شده به شکل ، ظرفیت و فشردگی رگ (یا لوله) بستگی ندارد.
بگذارید هنگام احتراق مخلوط در انتهای بسته ، انتقال از احتراق سریع به انفجار را در یک لوله طولانی از سطح مقطع ثابت در نظر بگیریم. تحت فشار جلوی شعله ، امواج فشرده سازی - امواج شوک - در مخلوط قابل احتراق ظاهر می شوند. در موج شوک ، دمای گاز تا مقادیری افزایش می یابد که در آن خود اشتعال مخلوط بسیار جلوتر از جلوی شعله رخ می دهد. به این حالت احتراق انفجار گفته می شود. با حرکت جلوی شعله ، حرکت لایه های مجاور دیوار مهار شده و بر این اساس ، حرکت مخلوط در مرکز لوله تسریع می شود. توزیع سرعت
رشد مقطعی ناهموار می شود. جت هایی از مخلوط های گازی وجود دارد که سرعت آنها کمتر از متوسط سرعت مخلوط گاز در هنگام احتراق طبیعی است و جت ها با سرعت بیشتری حرکت می کنند. در این شرایط ، سرعت شعله نسبت به مخلوط افزایش می یابد ، میزان سوزاندن گاز در واحد زمان افزایش می یابد و حرکت جلوی شعله با حداکثر سرعت جت گاز تعیین می شود.
با شتاب گرفتن شعله ، دامنه موج شوک نیز افزایش می یابد ، دمای فشرده سازی به دمای خود روشن شدن مخلوط می رسد.
افزایش مقدار کل گاز احتراق در واحد زمان با این واقعیت توضیح داده می شود که در یک جت با سرعت مقطع متغیر ، جلوی شعله خم می شود. در نتیجه این ، سطح آن افزایش می یابد و میزان ماده قابل احتراق به تناسب افزایش می یابد.
یکی از راه های کاهش میزان احتراق مخلوط های قابل احتراق ، عملکرد گازهای بی اثر بر روی شعله است ، اما به دلیل بازده پایین آنها ، در حال حاضر با افزودن هیدروکربن های هالوژنه به مخلوط ، از مهار احتراق شیمیایی استفاده می شود.
مخلوط های گاز قابل احتراق دارای دو درجه حرارت نظری احتراق هستند - در حجم ثابت و در فشار ثابت ، که اولی همیشه بالاتر از دومی است.
روش محاسبه دمای احتراق کالریمتری در فشار ثابت در بخش 1 در نظر گرفته شده است. بیایید روش محاسبه دمای احتراق نظری مخلوط های گاز را در یک حجم ثابت در نظر بگیریم ، که مربوط به انفجار در یک ظرف بسته است. محاسبه دمای احتراق نظری در حجم ثابت بر اساس همان شرایطی است که در Sec نشان داده شده است. 1.7
هنگامی که مخلوط های گاز در حجم بسته می سوزند ، محصولات احتراق کار نمی کنند. انرژی انفجار فقط برای گرم کردن محصولات انفجار صرف می شود. در این حالت ، کل انرژی به عنوان مجموع انرژی داخلی مخلوط انفجاری Q int.en.cm و گرمای احتراق ماده داده شده تعیین می شود. مقدار Q int.en.cm برابر است با مجموع محصولات ظرفیت گرمایی اجزای مخلوط انفجاری در حجم ثابت توسط دمای اولیه مخلوط
Q int.en.cm = s 1 T + s 2 T + ... + s n T ،
که در آن s 1 ، s 2 ، s n ظرفیت گرمایی ویژه اجزای سازنده مخلوط انفجاری ، kJ / (kg × K) است. T دمای اولیه مخلوط است ، K
مقدار Q int.en.cm را می توان در جداول مرجع یافت. دمای انفجار مخلوط های گاز در حجم ثابت با همان روش دمای احتراق مخلوط در فشار ثابت محاسبه می شود.
فشار انفجار از دمای انفجار پیدا می شود. فشار حین انفجار مخلوط گاز و هوا در حجم بسته به دمای انفجار و نسبت تعداد مولکول های محصولات احتراق به تعداد مولکول های مخلوط انفجاری بستگی دارد. در صورت انفجار مخلوط گاز و هوا ، اگر فشار اولیه مخلوط نرمال باشد ، فشار معمولاً از 1.0 مگاپاسکال بیشتر نمی شود. هنگام جایگزینی هوا در مخلوط انفجاری با اکسیژن ، از آنجا که دمای احتراق افزایش می یابد ، فشار انفجار به شدت افزایش می یابد.
در انفجار حتی یک مخلوط گاز و هوا استوکیومتری ، مقدار قابل توجهی گرما صرف گرم شدن نیتروژن مخلوط می شود ؛ بنابراین ، دمای انفجار چنین مخلوط هایی بسیار کمتر از دمای انفجار مخلوط با اکسیژن است. بنابراین ، فشار انفجار مخلوط استوکیومتری متان ، اتیلن ، استون و متیل اتر
ra با اکسیژن 1.5 - 1.9 مگاپاسکال است و مخلوط استوکیومتری آنها با هوا 1.0 مگاپاسکال است.
حداکثر فشار انفجار در محاسبات مقاومت در برابر انفجار تجهیزات و همچنین در محاسبات دریچه های ایمنی ، غشاهای انفجار و محفظه های تجهیزات الکتریکی ضد انفجار استفاده می شود.
فشار انفجار P انفجار (در MPa) مخلوط های گاز و هوا با فرمول محاسبه می شود
 ,
,
جایی که Р 0 - فشار اولیه مخلوط انفجاری ، MPa ؛ انفجار T 0 و T - دمای اولیه مخلوط انفجاری و دمای انفجار ، K ؛ - تعداد مولکول های گازهای حاصل از احتراق پس از انفجار ؛ - تعداد مولکولهای گازهای مخلوط قبل از انفجار.
مثال 4.1 ... فشار را هنگام انفجار مخلوط بخار الکل اتیل و هوا محاسبه کنید.
 .
.
P 0 = 0.1 مگاپاسکال ؛ T بزرگسال = 2933 K T 0 = 273 + 27 = 300 K؛ = 2 + 3 + 11.28 = 16.28 مول؛ = 1 + 3 + 11.28 = 15.28 مول.
آژانس فدرال آموزش فدراسیون روسیه
م institutionسسه آموزش عالی آموزش عالی حرفه ای
"دانشگاه فنی دولتی اوفا"
بخش "ایمنی صنعتی و حفاظت از کار"
کار آزمایشی با موضوع:
نظریه احتراق و انفجار
1. نظریه انفجار
در فرآیندهای فن آوری مرتبط با تولید ، حمل و نقل ، فرآوری ، دریافت ، ذخیره و استفاده از گازهای قابل اشتعال (GG) و مایعات قابل اشتعال (FL) ، همیشه خطر تشکیل گازهای انفجاری و مخلوط های بخار هوا وجود دارد.
یک محیط انفجاری می تواند توسط مخلوط مواد (گازها ، بخارات ، گرد و غبار) با هوا و سایر اکسیدان ها (اکسیژن ، ازن ، کلر ، اکسیدهای نیتروژن و غیره) و مواد مستعد تغییر شکل مواد منفجره (استیلن ، ازن ، هیدرازین و غیره) تشکیل شود. )
دلایل انفجار اغلب نقض قوانین مربوط به عملکرد ایمن تجهیزات ، نشت گاز از طریق نشت در اتصالات ، گرم شدن بیش از حد دستگاه ها ، افزایش فشار بیش از حد ، عدم کنترل مناسب فرآیند فن آوری ، پارگی یا خرابی قطعات تجهیزات است ، و غیره.
منبع شروع انفجار عبارتند از:
شعله های آتش باز ، اجسام سوزان و رشته ای
تخلیه الکتریکی
تظاهرات حرارتی واکنش های شیمیایی و تأثیرات مکانیکی ؛
جرقه های ناشی از ضربه و اصطکاک:
امواج شوک
تابش الکترومغناطیسی و سایر
طبق PB 09-540-03 ، یک انفجار عبارت است از:
I. فرآیند انتشار موقت انرژی بالقوه همراه با تغییر ناگهانی در حالت ماده و همراه با جهش فشار یا موج شوک.
2. آزاد سازی کوتاه مدت انرژی داخلی ، ایجاد فشار اضافی
انفجار می تواند با احتراق یا بدون احتراق (فرآیند اکسیداسیون) رخ دهد.
پارامترها و خصوصیات مشخص کننده انفجارپذیری محیط:
نقطه اشتعال ؛
محدودیت غلظت و دمای اشتعال ؛
دمای احتراق خودکار
گسترش طبیعی شعله ؛
حداقل محتوای اکسیژن منفجره (اکسید کننده) ؛
حداقل انرژی اشتعال ؛
حساسیت به تنش مکانیکی (ضربه و اصطکاک). عوامل خطرناک و مضر بر کارگران
در نتیجه انفجار ، موارد زیر است:
موج شوک ، که در جلوی آن فشار بیش از مقدار مجاز است.
در حال فرو ریختن سازه ها ، تجهیزات ، ارتباطات ، ساختمانها و سازه ها و قطعات پرواز آنها.
مواد خطرناکی که هنگام انفجار تشکیل شده و (یا) از تجهیزات آسیب دیده آزاد می شوند ، محتوای آنها در هوای منطقه کار بیش از حداکثر غلظت مجاز است.
عوامل اصلی مشخص کننده خطر انفجار:
حداکثر فشار و دمای انفجار ؛
سرعت افزایش فشار در هنگام انفجار ؛
فشار در جلوی موج شوک ؛
خرد کردن و خاصیت انفجاری زیاد محیط انفجاری.
در یک انفجار ، انرژی پتانسیل اولیه یک ماده ، به عنوان یک قاعده ، به انرژی گازهای فشرده گرم تبدیل می شود ، که به نوبه خود ، وقتی منبسط می شوند ، به انرژی حرکت ، فشرده سازی و گرمایش محیط تبدیل می شوند. بخشی از انرژی به صورت انرژی داخلی (حرارتی) گازهای منبسط شده باقی می ماند.
مقدار کل انرژی آزاد شده در هنگام انفجار ، پارامترهای کلی (حجم ، مساحت) تخریب را تعیین می کند. غلظت انرژی (انرژی در واحد حجم) شدت تخریب در کانون انفجار را تعیین می کند. این خصوصیات به نوبه خود به سرعت آزاد شدن انرژی توسط سیستم منفجره که باعث ایجاد موج انفجار می شود بستگی دارد.
انفجارها که بیشتر در روش تحقیق مشاهده می شوند ، می توانند به دو گروه اصلی تقسیم شوند: انفجارهای شیمیایی و فیزیکی.
انفجارهای شیمیایی شامل فرآیندهای تبدیل شیمیایی یک ماده است که با احتراق آشکار می شود و با آزاد شدن انرژی گرمایی در مدت زمان کوتاهی و در حدی از حجم مشخص می شود که امواج فشاری تشکیل شده و از منبع انفجار منتشر می شوند.
انفجارهای فیزیکی شامل فرایندهایی هستند که منجر به انفجار می شوند و با تغییرات شیمیایی یک ماده ارتباط ندارند.
انفجارهای تصادفی اغلب در اثر فرآیندهای احتراق ایجاد می شوند. انفجارهای این نوع اغلب در هنگام ذخیره سازی ، حمل و نقل و ساخت مواد منفجره (HE) اتفاق می افتد. آنها انجام می شوند:
هنگام دست زدن به مواد منفجره و مواد منفجره صنایع شیمیایی و پتروشیمی ؛
وقتی گاز طبیعی در ساختمانهای مسکونی نشت می کند ؛
در طول ساخت ، حمل و نقل و ذخیره سازی مواد قابل احتراق بسیار فرار یا مایع ؛
هنگام شستشوی مخازن ذخیره سوخت مایع ؛
در ساخت ، ذخیره و استفاده از سیستم های گرد و غبار قابل احتراق و برخی از مواد جامد و مایع خود به خود قابل احتراق.
ویژگی های انفجار شیمیایی
دو نوع انفجار اصلی وجود دارد: انفجار مواد منفجره متراکم و انفجار حجمی (انفجار بخارات گرد و غبار و مخلوط های گاز). انفجارهای مواد منفجره متراکم ناشی از تمام مواد منفجره جامد و تعداد نسبتاً کمی مواد منفجره مایع ، از جمله نیتروگلیسیرین است. چنین مواد منفجره معمولاً دارای چگالی 1300-1800 کیلوگرم بر متر مکعب هستند ، با این حال ، مواد منفجره اولیه حاوی سرب یا جیوه دارای تراکم بسیار بیشتری هستند.
واکنش های تجزیه:
ساده ترین حالت انفجار ، فرآیند تجزیه با تشکیل فرآورده های گازی است. به عنوان مثال ، تجزیه پراکسید هیدروژن با اثر حرارتی بالا و تشکیل بخار آب و اکسیژن:
2Н2О2 → 2Н2О2 + О2 + 106 کیلوژول / مول
پراکسید هیدروژن از غلظت 60٪ خطرناک است.
تجزیه در اثر اصطکاک یا تأثیر آزید سرب:
Pb (N3) 2 → Pb -u 3N2 + 474 kJ / mol.
ترینیتروتوولوئن (TNT) ماده ای با "کمبود اکسیژن" است و بنابراین یکی از محصولات اصلی پوسیدگی آن کربن است که در تشکیل دود در اثر انفجارهای TNT نقش دارد.
موادی که مستعد تجزیه انفجاری هستند تقریباً همیشه حاوی یک یا چند ساختار شیمیایی مشخص هستند که مسئول توسعه ناگهانی یک فرآیند با آزادسازی مقادیر زیادی انرژی هستند. این ساختارها شامل گروه های زیر است:
NO2 و NO3 - در مواد آلی و معدنی ؛
N = N-N - در آزیدهای آلی و معدنی ؛
NX3 ، جایی که X هالوژن است ،
N = C در فولمینات ها.
بر اساس قوانین ترموشیمی ، شناسایی ترکیباتی که روند تجزیه آنها می تواند انفجاری باشد امکان پذیر است. یکی از عوامل تعیین کننده که خطر بالقوه یک سیستم را تعیین می کند ، شیوع انرژی داخلی آن در حالت اولیه نسبت به حالت نهایی است. این شرایط در صورت جذب گرما (واکنش گرمازا) در هنگام تشکیل یک ماده برآورده می شود. مثالی از یک فرآیند مناسب ، تشکیل استیلن از عناصر است:
2C + H2 → CH = CH - 242 kJ / mol.
مواد غیر انفجاری که در هنگام تشکیل گرما از دست می دهند (واکنش گرمازا) شامل دی اکسید کربن است
С + О2 → СО2 + 394 kJ / mol.
باید در نظر داشت که استفاده از قوانین ترموشیمی تنها آشکار ساختن یک روند انفجاری را ممکن می سازد. اجرای آن به سرعت واکنش و تشکیل محصولات فرار بستگی دارد. بنابراین ، به عنوان مثال ، واکنش پارافین شمع با اکسیژن ، با وجود گرمازایی زیاد ، به دلیل سرعت کم منجر به انفجار نمی شود.
واکنش 2Аl + 4АС2О2 → Аl2О3 + 2Fе به خودی خود ، با وجود گرمازایی زیاد ، همچنین منجر به انفجار نمی شود ، زیرا هیچ محصول گازی تشکیل نمی شود.
واکنش های ردوکس ، که اساس واکنش های احتراق را تشکیل می دهند ، فقط در شرایط مطلوب برای دستیابی به سرعت بالای واکنش و افزایش فشار می توانند منجر به انفجار شوند. احتراق مواد جامد و مایعات بسیار پراکنده می تواند منجر به فشار بیش از حد تا 8 بار در یک محیط بسته شود. نسبتاً نادر است ، به عنوان مثال در سیستم های هوای مایع که آئروسل قطره قطره های روغن است.
واکنشهای پلیمریزاسیون گرمازا و وجود یک مونومر فرار اغلب به مرحله ای می رسند که افزایش خطرناک فشار ممکن است اتفاق بیفتد ، برای برخی از مواد مانند اکسید اتیلن ، پلیمریزاسیون می تواند در دمای اتاق شروع شود ، به ویژه هنگامی که ترکیبات شروع به شتاب دهنده های پلیمریزاسیون آلوده شوند. اکسید اتیلن همچنین می تواند به صورت گرمازایی به استالدئید ایزومری شود:
CH2CH2O - CH3HC = O + 113.46 کیلوژول در مول
واکنش های متراکم به طور گسترده ای در تولید رنگ ، لاک و رزین استفاده می شود و به دلیل گرمازایی فرآیند و وجود اجزای فرار ، گاهی منجر به انفجار می شود.
برای روشن کردن شرایط عمومی مطلوب برای شروع احتراق و انتقال آن به یک انفجار ، نمودار (شکل 1) وابستگی به درجه حرارت توسعه یافته در سیستم قابل احتراق را در مقابل زمان در حضور تولید گرمای حجمی با آن به دلیل مواد شیمیایی در نظر بگیرید واکنش و از دست دادن گرما.
اگر دمای T1 را روی نمودار به عنوان یک نقطه حساس که در آن احتراق در سیستم رخ می دهد ، نشان دهیم ، بدیهی می شود که در شرایطی که بیش از حد از دست دادن گرما بیش از ورودی گرما باشد ، چنین احتراقی رخ نمی دهد. این فرآیند تنها زمانی آغاز می شود که برابری بین میزان آزاد سازی گرما و از دست دادن گرما (در نقطه مماس منحنی های مربوطه) حاصل شود و با افزایش دما و. بنابراین ، فشار قبل از انفجار.
بنابراین ، در صورت وجود شرایط مطلوب برای عایق حرارتی ، وقوع یک واکنش گرمازا در یک سیستم قابل احتراق می تواند علاوه بر احتراق ، منجر به انفجار نیز شود.
واکنشهای کنترل نشده ای که به نفع انفجار بوجود می آیند به این دلیل است که سرعت انتقال حرارت ، به عنوان مثال به عروق ، یک تابع خطی از اختلاف دما بین جرم واکنش و ماده خنک کننده است ، در حالی که میزان واکنش گرمازا و ، بنابراین ، جریان گرما از آن مطابق قانون قدرت ، با افزایش غلظت های اولیه واکنش دهنده ها رشد می کند و با افزایش دما در نتیجه وابستگی نمایی میزان واکنش شیمیایی به دما ، به سرعت افزایش می یابد (قانون آرنیوس ) این قوانین کمترین میزان احتراق مخلوط و دما را در حد غلظت پایین تر احتراق تعیین می کند. با نزدیک شدن غلظت سوخت و اکسید کننده به استوکیومتری ، سرعت سوزش و دما به حداکثر مقادیر افزایش می یابد.
غلظت گاز استوکیومتری غلظت گاز قابل احتراق در مخلوطی با یک محیط اکسید کننده است که در آن از یک تعامل شیمیایی کامل سوخت و اکسید کننده مخلوط اطمینان حاصل می شود.
3. ویژگی های انفجار فیزیکی
انفجارهای فیزیکی معمولاً با انفجار عروق ناشی از فشار بخار و شیارها همراه هستند. علاوه بر این ، دلیل اصلی تشکیل آنها یک واکنش شیمیایی نیست ، بلکه یک فرایند فیزیکی است که به دلیل آزاد شدن انرژی داخلی گاز فشرده یا مایع است. قدرت چنین انفجارهایی به فشار داخلی بستگی دارد و تخریب ناشی از موج ضربه ای از گاز در حال انبساط یا ترکش های یک رگ پارگی است. اگر به عنوان مثال یک سیلندر گاز تحت فشار قابل حمل سقوط کرده و یک شیر آزادی فشار از بین برود ، می تواند یک انفجار فیزیکی رخ دهد. فشارهای LPG به ندرت از 40 بار فراتر می رود (فشار حیاتی اکثر LPG های معمولی).
انفجارهای فیزیکی همچنین شامل پدیده اصطلاحاً انفجار فیزیکی است. این پدیده زمانی اتفاق می افتد که مایعات سرد و گرم با هم مخلوط شوند ، زمانی که دمای یکی از آنها به طور قابل توجهی بالاتر از نقطه جوش دیگری باشد (به عنوان مثال ریختن فلز مذاب در آب). در مخلوط بخار و مایع حاصل ، بخاطر فرآیندهای در حال رشد ریز بلغم سازی قطرات مذاب ، حذف سریع گرما از آنها و گرم شدن بیش از حد مایع سرد با تبخیر شدید ، تبخیر می تواند به صورت انفجاری پیش برود.
انفجار فیزیکی با ظهور یک موج شوک با فشار بیش از حد در فاز مایع همراه است و در بعضی موارد به بیش از هزار اتمسفر می رسد. بسیاری از مایعات در شرایطی ذخیره می شوند یا استفاده می شوند که فشار بخار آنها به طور قابل توجهی بالاتر از جو باشد. این مایعات عبارتند از: گازهای قابل اشتعال مایع (به عنوان مثال پروپان ، بوتان) مبرد مایع آمونیاک یا فریون که در دمای اتاق ذخیره می شود ، متان ، که باید در دمای پایین تر ، آب گرم شده در دیگهای بخار ذخیره شود. اگر ظرفی با مایع بیش از حد گرم صدمه ببیند ، در این صورت جریان بخار به فضای اطراف و تبخیر جزئی سریع مایعات وجود دارد. با یک خروج سریع و سریع بخار ، امواج انفجار در محیط تولید می شوند. دلایل انفجار شناورها با گازها و بخارات تحت فشار عبارتند از:
نقض یکپارچگی پرونده به دلیل خرابی هر واحد ، آسیب یا خوردگی در اثر عملکرد نادرست ؛
گرم شدن بیش از حد رگ به دلیل نقض در گرمایش الکتریکی یا نحوه عملکرد دستگاه احتراق (در این حالت ، فشار داخل رگ افزایش می یابد و قدرت بدن به حالت آسیب دیده کاهش می یابد) ؛
انفجار رگ هنگام عبور از فشار مجاز.
انفجار ظروف گاز با احتراق بعدی در جو اساساً همان دلایلی را دارد که در بالا توضیح داده شد و مشخصه انفجارهای فیزیکی است. تفاوت اصلی در تشکیل در این مورد از یک گلوله آتشین است ، که اندازه آن به مقدار سوخت گازی ساطع شده در جو بستگی دارد. این مقدار به نوبه خود به حالت فیزیکی گاز در ظرف بستگی دارد. وقتی سوخت در حالت گازی باشد ، مقدار آن بسیار کمتر از ذخیره سازی در همان ظرف به شکل مایع خواهد بود. پارامترهای انفجار که عواقب آن را تعیین می کنند عمدتا توسط ماهیت توزیع انرژی در منطقه انفجار و توزیع آن هنگام انتشار موج انفجار از منبع انفجار تعیین می شود.
4. پتانسیل انرژی
انفجار بسیار مخرب است. مهمترین ویژگی انفجار ، کل انرژی یک ماده است. این شاخص پتانسیل انرژی انفجاری نامیده می شود ، در تمام پارامترهای توصیف کننده مقیاس و پیامدهای انفجار وجود دارد.
در صورت کاهش فشار اضطراری دستگاه ، افشای کامل (تخریب) آن اتفاق می افتد.
مساحت نشت مایعات بر اساس راه حلهای طراحی ساختمانها یا یک سایت در فضای باز تعیین می شود.
زمان تبخیر بیش از 1 ساعت طول نمی کشد:
E = EII1 + EII2 + EII1 + EII2 + EII3 + EII4 ،
انفجار خطر اتاق آتش نشان
که در آن EI1 مجموع انرژی انبساط آدیاباتیک و احتراق فاز گاز بخار است (PHPC به طور مستقیم در بلوک قرار دارد ، kJ ؛
EI2 انرژی احتراقی GPF است که از اشیا blocks مجاور (بلوک ها) ، kJ به بخش کم فشار عرضه می شود.
EII1 انرژی احتراق GTHF است که به دلیل انرژی LF بیش از حد گرم بلوک مورد بررسی و از اشیا adj مجاور ، kJ تأمین می شود.
EII2 انرژی احتراق PHF است که از فاز مایع (LF) به دلیل گرمای واکنش های گرمازایی ایجاد می شود که در طول فشار خون متوقف نمی شوند ، kJ.
EII3 انرژی احتراق PGF است. از فاز مایع به دلیل ورود گرما از حامل های حرارتی خارجی ، kJ تشکیل شده است.
EII4 انرژی احتراق PHF تولید شده از LF است که به دلیل انتقال گرما از محیط (از سطح جامد و هوا ، به مایع در امتداد سطح آن) به سطح جامد (کف ، مخزن ، خاک و غیره) ریخته می شود ، کیلوژول .
مقادیر پتانسیل های انرژی کلی خطر انفجار برای تعیین مقادیر جرم کاهش یافته و پتانسیل انرژی نسبی ، که مشخصه خطر انفجار واحدهای فناوری است ، استفاده می شود.
جرم کاهش یافته مجموع جرم بخارات قابل احتراق (گازها) یک ابر گاز بخار قابل انفجار است که به یک انرژی احتراق خاص برابر با 46000 کیلوژول بر کیلوگرم کاهش می یابد:
پتانسیل نسبی انرژی خطر انفجار Qv واحد فناوری ، که ویژگی کل انرژی احتراق است و می تواند با استفاده از روش محاسبه مطابق فرمول محاسبه شود:
![]()
که در آن E کل پتانسیل انرژی خطر انفجار واحد فناوری است.
بر اساس مقادیر پتانسیل های انرژی نسبی Ov به جرم کاهش یافته ماده بخار گاز بخار متر ، بلوک های فرآیند دسته بندی می شوند. شاخص های گروه خطر انفجار واحدهای فناوری در جدول 1 نشان داده شده است.
جدول شماره
| دسته انفجار | Ov | متر |
| من | >37 | >5000 |
| دوم | 27 − 37 | 2000−5000 |
| III | <27 | <2000 |
5. معادل TNT. فشار بیش از حد در جلو شوک
روش معادل TNT به طور گسترده ای برای ارزیابی سطح تأثیر اختلالات تصادفی و عمدی استفاده می شود. طبق این روش ، درجه تخریب با معادل TNT مشخص می شود ، جایی که جرم TNT ، که برای ایجاد یک سطح تخریب مشخص مورد نیاز است ، تعیین می شود. معادل TNT انفجار یک محیط بخار گاز Wt ( کیلوگرم) با توجه به شرایط کافی بودن ماهیت و درجه تفکیک در انفجارهای ابرهای گاز بخار ، و همچنین ترکیبات شیمیایی و مایع ناپایدار جامد و مایع ، تعیین شده توسط فرمول ها تعیین می شود:
1 برای محیط های بخار و گاز
![]()
q / - گرمای ویژه احتراق محیط گاز بخار ، کیلوگرم کیلوگرم ،
qT - انرژی انفجار اختصاصی TNT kJ / kg.
2 برای ترکیبات ناپایدار شیمیایی جامد و مایع
![]()
جایی که Wk جرم ترکیبات جامد و مایع شیمیایی ناپایدار است. qk انرژی انفجار ویژه ترکیبات ناپایدار شیمیایی جامد و مایع است. در تولید ، انفجار مخلوط گاز-هوا ، بخار-هوا یا گرد و غبار موج ضربه ایجاد می کند. درجه وضوح سازه های ساختمان ، تجهیزات ، ماشین آلات و ارتباطات ، و همچنین آسیب به افراد بستگی به فشار اضافی در مقابل موج شوک ΔРФ (تفاوت بین حداکثر فشار در مقابل موج شوک و فشار جوی طبیعی جلوتر از این جبهه).
محاسبات برای ارزیابی عملکرد گازهای شیمیایی قابل اشتعال و مایعات به تعیین فشار بیش از حد در مقابل شوک (ΔРФ) در طول انفجار مخلوط گاز و هوا در یک فاصله مشخص از ظرف که مقدار مشخصی از یک مخلوط مواد منفجره در آن کاهش می یابد ، کاهش می یابد ذخیره شده.
6. محاسبه برای تعیین فشار بیش از حد انفجار
محاسبه فشار بیش از حد انفجار برای گازهای قابل احتراق ، بخارات مایعات قابل اشتعال و قابل اشتعال مطابق با روش تعیین شده در NPB 105-03 "تعیین دسته بندی مکان ها ، ساختمانها و تاسیسات بیرونی برای انفجار و خطر آتش سوزی" انجام می شود.
وظیفه: برای تعیین فشار بیش از حد ناشی از انفجار سولفید هیدروژن در اتاق.
شرایط پایه
هیدروژن به طور دائم در دستگاه 20 متر مکعب ذخیره می شود. دستگاه در کف قرار دارد. طول کل خطوط لوله با قطر 50 میلی متر ، محدود شده توسط دریچه ها (دستی) نصب شده بر روی بخشهای ورودی و خروجی خطوط لوله ، 15 متر است. سرعت جریان سولفید هیدروژن در خطوط لوله 4 · 10-3 متر مکعب است s ابعاد اتاق 10x10x4 متر است.
این اتاق دارای تهویه اضطراری با نرخ تبادل هوا 8 ساعت در 1 است. تهویه اضطراری با فن های پشتیبان ، راه اندازی اتوماتیک در صورت عبور از حداکثر غلظت انفجار مجاز و منبع تغذیه با توجه به قابلیت اطمینان دسته اول (PUE) تأمین می شود. دستگاه های خارج كردن هوا از اتاق در نزدیكی محل حادثه احتمالی قرار دارند.
سازه های اصلی ساختمان از بتن مسلح است.
توجیه گزینه طراحی
طبق NPB 105-03 ، نامطلوب ترین سناریو تصادف باید به عنوان سناریوی محاسبه شده تصادف در نظر گرفته شود ، که در آن بیشترین مقدار موادی که در رابطه با عواقب انفجار خطرناک ترین هستند درگیر هستند.
و بعنوان یک گزینه طراحی ، گزینه کاهش فشار کانتینر با سولفید هیدروژن و خروج از آن و خطوط لوله انتقال و خروجی سولفید هیدروژن به حجم اتاق اتخاذ شد.
1) فشار انفجار بیش از حد برای مواد احتراق منفرد متشکل از اتم C ، H ، O ، N ، Cl ، Br ، I ، F با فرمول تعیین می شود
 (1)
(1)
حداکثر فشار انفجار مخلوط گاز-هوا یا بخار-هوای استوکیومتری در یک حجم بسته ، که به صورت آزمایشی یا مطابق با داده های مرجع مطابق با الزامات بند 3 NPB-105-03 تعیین شده است ، کجاست؟ در غیاب داده ها ، مجاز به گرفتن 900 kPa است.
فشار اولیه ، kPa (مجاز است برابر با 101 kPa گرفته شود) ؛
جرم گاز قابل احتراق (GG) یا بخارهای قابل اشتعال (FL) و مایعات قابل احتراق (GF) که در نتیجه حادثه به داخل اتاق رها شده اند ، کیلوگرم ؛
ضریب مشارکت سوخت در انفجار ، که می تواند براساس ماهیت توزیع گازها و بخارات در حجم اتاق مطابق پیوست محاسبه شود. طبق جدول مجاز است مقدار را بگیریم. 2 NPB 105-03. من آن را برابر با 0.5 می گیرم
حجم رایگان اتاق ،
دمای طراحی به عنوان حداکثر دمای مطلق هوا برای Ufa ، برابر با 39 درجه سانتیگراد در نظر گرفته شده است (طبق SNiP 23-01-99 "اقلیم شناسی ساخت").
در زیر محاسبه مقادیر لازم برای تعیین فشار اضافی انفجار سولفید هیدروژن در یک اتاق آمده است.
تراکم سولفید هیدروژن در دمای طراحی:
که در آن M جرم مولی سولفید هیدروژن است ، 34.08 کیلوگرم در کیلومتر.
v0 - حجم مولی برابر 22.413 متر مکعب در کیلومتر است.
0.00367 - ضریب انبساط حرارتی ، درجه -1 ؛
tp - دمای طراحی ، 390C (حداکثر دمای مطلق هوا برای Ufa).
غلظت استوکیومتری سولفید هیدروژن با فرمول محاسبه می شود:
![]() ;
;
جایی که β ضریب استوکیومتری اکسیژن در واکنش احتراق است.
![]()
nc ، nн ، n0 ، nх ، تعداد اتمهای C ، H ، O و هالوژنهای یک مولکول سوخت است.
برای سولفید هیدروژن (H2S) nc = 1 ، nn = 4 ، n0 = 0 ، nх = 0 ، بنابراین ،
با جایگزینی مقدار پیدا شده β ، مقدار غلظت استوکیومتری سولفید هیدروژن را بدست می آوریم:

حجم سولفید هیدروژن که در حادثه طراحی وارد اتاق شده است شامل حجم گاز خارج شده از دستگاه و حجم گاز خارج شده از خط لوله قبل از بسته شدن سوپاپ ها و بعد از بسته شدن سوپاپ ها است:
جایی که Va حجم گاز آزاد شده از دستگاه است ، m3 ؛
V1T - حجم گاز آزاد شده از خط لوله قبل از خاموش شدن ، m3 ؛
V2T حجم گاز آزاد شده از خط لوله پس از خاموش شدن آن است ، m3 ؛
که در آن q سرعت جریان مایع است که مطابق با مقررات فن آوری تعیین می شود ، m3 / s ؛
T مدت زمان جریان گاز در حجم اتاق است که مطابق با بند 38 NPB 105-03 s تعیین می شود.
جایی که d قطر داخلی خطوط لوله است ، متر ؛
Ln طول خطوط لوله از دستگاه اضطراری به سوپاپ ها ، متر است.
بنابراین ، در صورت سناریوی تصادف در نظر گرفته شده ، حجم سولفید هیدروژن وارد اتاق می شود:
جرم سولفید هیدروژن در اتاق:
در صورت گردش گازهای قابل اشتعال ، گازهای قابل اشتعال یا قابل احتراق ، مایعات قابل اشتعال یا قابل اشتعال در اتاق ، هنگام تعیین مقدار جرم ، مجاز است که در صورت تهویه اضطراری ، تهویه اضطراری را نیز در نظر بگیرید ، هنگامی شروع به کار کنید که از حداکثر غلظت مجاز ضد انفجار فراتر رفته و منبع تغذیه مطابق با قابلیت اطمینان دسته اول (PUE) ارائه شود ، مشروط بر اینکه دستگاه هایی برای حذف هوا از اتاق در مجاورت محل وقوع یک حادثه احتمالی قرار داشته باشند.
در این حالت ، توده گازهای قابل احتراق یا بخارات مایعات قابل اشتعال یا قابل احتراق که تا نقطه اشتعال و بالاتر گرم می شوند ، وارد حجم اتاق می شوند ، باید با ضریب تعیین شده توسط فرمول تقسیم شود
نرخ تبادل هوا که در اثر تهویه اضطراری ایجاد می شود ، در هر ثانیه کجاست؟ این اتاق دارای تهویه با نرخ تبادل هوا 8 (0.0022s) است.
مدت زمان جریان گازهای قابل اشتعال و بخارات مایعات قابل اشتعال و قابل احتراق به حجم اتاق ، ثانیه را می گیرم 300 ثانیه. (بند 7 NPB 105-03)
جرم سولفید هیدروژن در اتاق طی سناریوی تصادف در نظر گرفته شده:
![]()
نتایج محاسبه انفجار
| گزینه شماره | گاز قابل اشتعال |
مقدار ، kPa | ||
| سولفید هیدروژن | 5 | آسیب متوسط به ساختمانها | ||
جدول. حداکثر فشار بیش از حد مجاز در هنگام احتراق مخلوط های گاز ، بخار یا گرد و غبار هوا در اتاق ها یا در فضای باز
داده های اولیه و محاسبه شده در جدول 2 خلاصه شده است.
جدول 2 - داده های اولیه و محاسبه شده
| P / p No. | نام | تعیین | کمیت |
| 1 | ماده ، نام و فرمول آن | سولفید هیدروژن | H2S |
| 2 | وزن مولکولی ، کیلوگرم کیلومتر -1 | م | 34,08 |
| 3 | تراکم مایع ، کیلوگرم در متر مکعب | ρzh | - |
| 4 | تراکم گاز در دمای طراحی ، کیلوگرم در متر مکعب | ρg | 1,33 |
| 5 | دمای محیط (هوا قبل از انفجار) ، 0С | T0 | 39 |
| 6 | فشار بخار اشباع شده ، kPa | NS | 28,9 |
| 7 | غلظت استوکیومتری ،٪ vol. | Sst | 29,24 |
| 8 | ابعاد اتاق - طول ، متر - عرض ، متر - قد ، متر |
||
| 9 | ابعاد خط لوله: - قطر ، متر طول ، متر |
||
| 10 | مصرف هپتان در خط لوله ، m3 / s | س | 4 10-3 |
| 11 | زمان بسته شدن شیر دریچه ، s | تی | 300 |
| 12 | میزان تهویه اضطراری ، 1 در ساعت | آ | 8 |
| 13 | حداکثر فشار انفجار ، kPa | Pmax | 900 |
| 14 | فشار اولیه ، kPa | P0 | 101 |
| 15 | نشت و ضریب غیر آدیاباتیک | نان | 3 |
| 16 | ضریب مشارکت سوخت در انفجار | ز | 0,5 |
طبق NPB 105-2003 ، مقوله های محل انفجار و آتش سوزی مطابق با جدول 4 پذیرفته می شوند.
| دسته بندی اتاق | مشخصات مواد و موادی که در اتاق (در گردش) قرار دارند |
آتش سوزی و انفجار |
گازهای قابل احتراق ، مایعات قابل اشتعال با نقطه اشتعال بیش از 28 درجه سانتیگراد به اندازه ای که بتوانند مخلوط انفجاری بخار-گاز-هوا را ایجاد کنند ، در صورت احتراق ، فشار انفجار اضافی محاسبه شده در اتاق بیش از 5 کیلو پاسکال ایجاد می شود. مواد و موادی که می توانند هنگام تعامل با آب ، اکسیژن اتمسفر یا با یکدیگر به اندازه ای منفجر شوند و بسوزند که فشار اضافی محاسبه شده انفجار در اتاق بیش از 5 کیلو پاسکال باشد. |
|
انفجار و آتش سوزی خطرناک است |
گرد و غبار و الیاف قابل اشتعال ، مایعات قابل اشتعال با نقطه اشتعال بیش از 28 درجه سانتیگراد ، مایعات قابل اشتعال به میزان زیادی که در صورت اشتعال ، فشار اضافی محاسبه شده انفجار در محفظه را تشکیل دهند ، می توانند مخلوط غبار منفجره هوا یا بخار هوا را ایجاد کنند. اتاق ، بیش از 5 کیلو پاسکال ، توسعه می یابد. |
| آتش سوزی B1-B4 خطرناک است | مایعات قابل اشتعال و به سختی قابل اشتعال ، مواد قابل احتراق جامد و به سختی قابل احتراق (از جمله گرد و غبار و الیاف) ، مواد و موادی که فقط در صورت تعامل با آب ، اکسیژن هوا یا با یکدیگر می توانند بسوزند ، به شرطی که محل هایی که در آن موجود است یا در گردش ، به دسته A یا B تعلق ندارند. |
| G | مواد و مواد غیر قابل احتراق در حالت گرم ، رشته ای یا ذوب ، که پردازش آنها با آزاد شدن گرمای تابشی ، جرقه ها و شعله همراه است. گازهای قابل اشتعال ، مایعات و جامداتی که می سوزند یا به عنوان سوخت دفع می شوند. |
| د | مواد و مواد غیر قابل اشتعال در حالت سرد ، |
نتیجه گیری: این اتاق به گروه A تعلق دارد ، زیرا امکان انتشار گاز قابل اشتعال (سولفید هیدروژن) به اندازه ای وجود دارد که بتواند در صورت اشتعال ، فشار اضافی محاسبه شده انفجار را در صورت ایجاد مخلوط انفجاری بخار - گاز هوا ایجاد کند. اتاق ، بیش از 5 کیلو پاسکال ، توسعه می یابد.
8. تعیین مقادیر شاخص های انرژی خطر انفجار واحد فناوری در هنگام انفجار
پتانسیل انرژی انفجاری E (kJ) واحد با در نظر گرفتن مقدار کار انبساط آدیاباتیک آن و همچنین مقدار آن ، توسط کل انرژی احتراق فاز گاز بخار واقع در واحد تعیین می شود. انرژی احتراق کامل مایع تبخیر شده از حداکثر سطح ممکن تنگه آن ، در حالی که در نظر گرفته شده است:
1) در صورت فشار اضطراری دستگاه ، افشای کامل (تخریب) آن اتفاق می افتد ؛
2) مساحت نشت مایع بر اساس راه حل های طراحی ساختمان ها یا یک سایت در فضای باز تعیین می شود.
3) زمان تبخیر بیش از 1 ساعت طول نمی کشد:
مجموع انرژی انبساط آدیاباتیک A (kJ) و احتراق PGF واقع در بلوک ، kJ:
q "= 23380 کیلوژول بر کیلوگرم - گرمای احتراق ویژه PGF (سولفید هیدروژن) ؛
26.9 - جرم گاز قابل احتراق
 .
.
برای تعیین عملی انرژی انبساط آدیاباتیک PHF ، می توان از فرمول استفاده کرد
جایی که b1 - می تواند از جدول گرفته شود. 5. با نماد آدیاباتیک k = 1.2 و فشار 0.1 مگاپاسکال ، برابر با 40/1 است.
جدول 5. مقدار ضریب b1 بسته به شاخص آدیاباتیک محیط و فشار در واحد فناوری
| فهرست مطالب | فشار سیستم ، MPa | |||||||||
| آدیابات | 0,07-0,5 | 0,5-1,0 | 1,0-5,0 | 5,0-10,0 | 10,0-20,0 | 20,0-30,0 | 30,0-40,0 | 40,0-50,0 | 50,0-75,0 | 75,0-100,0 |
| k = 1.1 | 1,60 | 1,95 | 2,95 | 3,38 | 3,08 | 4,02 | 4,16 | 4,28 | 4,46 | 4,63 |
| k = 1.2 | 1,40 | 1,53 | 2,13 | 2,68 | 2,94 | 3,07 | 3,16 | 3,23 | 3,36 | 3,42 |
| k = 1.3 | 1,21 | 1,42 | 1,97 | 2,18 | 2,36 | 2,44 | 2,50 | 2,54 | 2,62 | 2,65 |
| k = 1.4 | 1,08 | 1,24 | 1,68 | 1,83 | 1,95 | 2,00 | 2,05 | 2,08 | 2,12 | 2,15 |
0 کیلوژول انرژی احتراقی PGF است که از اشیا adj مجاور (بلوک ها) ، کیلوژول به قسمت کم فشار وارد می شود. هیچ بلوک مجاور وجود ندارد ، بنابراین این جز component صفر است.
0 کیلوژول انرژی احتراق PHF است که به دلیل انرژی LF بیش از حد گرم بلوک در نظر گرفته شده و در طی زمان ti از اجسام مجاور دریافت می شود.
0 کیلوژول انرژی احتراق PHF است که از LP به دلیل گرمای واکنش های گرمازا ایجاد می شود که در طول فشار زدایی متوقف نمی شوند.
0 کیلوژول انرژی احتراق PHF تولید شده از LP به دلیل ورودی گرما از حامل های حرارتی خارجی است.
0 کیلوژول انرژی احتراق PHF تولید شده از LP است که به دلیل انتقال گرما از محیط (از سطح جامد و هوا به مایع در امتداد سطح آن) بر روی یک سطح جامد (کف ، مخزن ، خاک و غیره) ریخته می شود.
پتانسیل انرژی خطر انفجار واحد:
E = 628923.51 kJ.
مقادیر پتانسیل انرژی کلی خطر انفجار E برای تعیین مقادیر جرم کاهش یافته و پتانسیل انرژی نسبی استفاده می شود که مشخصه خطر انفجار واحدهای فناوری است.
مجموع جرم بخارات قابل احتراق (گازها) یک ابر گاز بخار قابل انفجار ، t ، به یک انرژی احتراق خاص برابر با 46000 کیلوژول بر کیلوگرم کاهش می یابد:
![]()
پتانسیل انرژی نسبی خطر انفجار Qw واحد فناوری با استفاده از روش محاسبه مطابق فرمول پیدا می شود
بر اساس مقادیر پتانسیل های انرژی نسبی Qw و جرم کاهش یافته ماده بخار گاز بخار متر ، واحدهای فرآیند دسته بندی می شوند. شاخص های دسته ها در جدول آورده شده است. پنج
جدول 4. شاخص های گروه های خطر انفجار واحدهای فناوری
| دسته انفجار | پرسش | متر ، کیلوگرم |
| من | > 37 | > 5000 |
| دوم | 27 - 37 | 2000 - 5000 |
| III | < 27 | < 2000 |
نتیجه گیری: این اتاق به گروه III خطر انفجار تعلق دارد ، زیرا مجموع جرم ابر منفجره گاز بخار سولفید هیدروژن ، که به یک انرژی خاص احتراق کاهش می یابد ، 16.67 کیلوگرم است ، پتانسیل انرژی نسبی خطر انفجار 18/5 است. .
9. محاسبه غلظت انفجاری مخلوط گاز و هوا در اتاق. تعیین کلاس مکان برای انفجار و خطر آتش سوزی مطابق با PUE
بگذارید ما حجم غلظت انفجاری سولفید هیدروژن را در اتاق مشخص کنیم:
جایی که m جرم مخلوط بخار هوا در اتاق است ، کیلوگرم ،
NKPV - حد پایین غلظت احتراق ، g / m3.
غلظت مخلوط بخار هوا در اتاق:
![]()
جایی که VCM حجم غلظت انفجاری سولفید هیدروژن در اتاق است ، m3 ، VC6 حجم آزاد اتاق ، m3 است.
نتایج محاسبه در جدول 6 ارائه شده است.
جدول 6. نتایج محاسبه غلظت مخلوط گاز و هوا
طبق PUE ، اتاق مورد نظر متعلق به کلاس B-Ia است - مناطق واقع در اتاقهایی که در آن ، هنگام کار عادی ، مخلوط انفجاری گازهای قابل اشتعال (صرف نظر از حد پایین اشتعال) یا بخارات مایعات قابل اشتعال با هوا تشکیل نشده است ، اما فقط در اثر حوادث و سو mal عملکرد ممکن است.
10. تعیین مناطق تخریب در یک انفجار. طبقه بندی مناطق تخریب
شعاع مناطق تخریب در هنگام انفجار مخلوط گاز و هوا با توجه به روش شرح داده شده در ضمیمه 2 PB 09-540-03 تعیین شد.
جرم مواد گاز بخار (کیلوگرم) شرکت کننده در انفجار توسط محصول تعیین می شود
که z کسری از جرم کاهش یافته سولفید هیدروژن است که در انفجار شرکت می کند (برای GG برابر با 0.5 است) ،
t جرم سولفید هیدروژن در اتاق است ، کیلوگرم.
از معادل TNT می توان برای ارزیابی میزان تأثیر انفجار استفاده کرد. TNT معادل انفجار یک محیط بخار گاز بخار WT (کیلوگرم) با توجه به شرایط کافی بودن ماهیت و درجه تخریب در هنگام انفجار ابرهای گاز بخار ، و همچنین ترکیبات شیمیایی و مایع ناپایدار مایع تعیین می شود.
برای محیط های گاز-بخار ، TNT معادل انفجار محاسبه می شود:
که در آن 0.4 کسری از انرژی انفجار محیط گاز بخار است که به طور مستقیم در تشکیل موج شوک صرف می شود.
0.9 کسری از انرژی انفجار trinitrotoluene (TNT) است که مستقیماً در تشکیل موج شوک صرف می شود.
q "- گرمای احتراق احتراق محیط گاز بخار ، kJ / kg ؛
qT - انرژی انفجار اختصاصی TNT ، kJ / kg.
منطقه تخریب منطقه ای با مرزهای تعریف شده توسط شعاع R است که مرکز آن بلوک فناوری در نظر گرفته شده یا محتمل ترین مکان کاهش فشار سیستم فناوری است. مرزهای هر منطقه با مقادیر فشارهای اضافی در امتداد جلوی موج شوک AR و بر این اساس ، با ضریب بدون بعد K. مشخص می شود. طبقه بندی مناطق تخریب در جدول 6 آورده شده است.
جدول 7. میزان تخریب احتمالی در هنگام تغییر انفجاری ابرهای مخلوط های سوخت و هوا
| کلاس منطقه تخریب | ΔР، kPa | به | منطقه تخریب | خصوصیات منطقه آسیب دیده |
| 1 | ≥100 | 3,8 | پر شده | تخریب و ریزش همه عناصر ساختمانها و سازه ها ، از جمله زیرزمین ها ، درصد افراد زنده مانده است. برای ساختمانهای اداری و تاسیساتی و ساختمانهای مدیریت طراحی معمولی - 30٪ ؛ برای ساختمانهای صنعتی و سازه های معمولی - 0٪. |
| 2 | 70 | 5,6 | قوی | تخریب بخشی از دیوارها و سقف طبقات فوقانی ، ایجاد ترک در دیوارها ، تغییر شکل کف طبقات پایین. استفاده محدود از انبارهای زنده مانده پس از پاکسازی ورودی ها. درصد بقا در افراد: برای ساختمانهای اداری و تاسیساتی و ساختمانهای مدیریت طراحی معمولی - 85٪: برای ساختمانهای صنعتی و سازه های معمولی - 2٪ |
| 3 | 28 | 9,6 | وسط | تخریب عناصر عمدتا ثانویه (سقف ها ، پارتیشن ها و پر کردن درها). همپوشانی ها ، به عنوان یک قاعده ، از بین نمی روند. برخی از محل ها پس از پاکسازی آوار و انجام تعمیرات برای استفاده مناسب هستند. درصد بقا: -برای ساختمانهای اداری و تاسیساتی و ساختمانهای معمولی مدیریتی - 94٪. |
| 4 | 14 | 28 | ضعیف | تخریب پر کردن و پارتیشن پنجره و درب. زیرزمین ها و طبقات زیرین پس از تمیز کردن بقایا و پر کردن دهانه ها کاملاً حفظ شده و برای استفاده موقت مناسب هستند. درصد بقا از مردم: - برای ساختمانهای اداری و راحتی و ساختمانهای معمولی مدیریت - 98٪. ساختمانهای صنعتی و سازه های معمولی - 90٪ |
| 5 | ≤2 | 56 | لعاب | تخریب پر کردن شیشه. درصد افرادی که زنده مانده اند - 100٪ |
شعاع منطقه تخریب (متر) به صورت کلی با عبارت تعیین می شود:

که در آن K یک ضریب بدون بعد است که توصیف کننده تأثیر انفجار بر روی یک جسم است.





نتایج محاسبه شعاع مناطق تخریب در هنگام انفجار مخلوط سوخت و هوا در اتاق در جدول 7 ارائه شده است.
جدول 7 - نتایج محاسبه شعاع مناطق تخریب
لیست منابع استفاده شده
1. Beschastnov M.V. انفجارهای صنعتی ارزیابی و هشدار. - M. شیمی ، 1991
2. ایمنی زندگی ، ایمنی فرآیندهای فن آوری و تولید (حمایت از کار): کتاب درسی ، کتابچه راهنمای دانشگاه ها / PP Kukin ، V.L. لاپین ، N ، L. پونوماروف و دیگران ، - م. ،: بالاتر. sc.t 2001 ،
3. PB 09-540-03 "قوانین عمومی ایمنی در برابر انفجار برای صنایع شیمیایی ، پتروشیمی و پالایش نفت و مواد خطرناک برای آتش سوزی و آتش سوزی."
4. GOST 12.1،010-76 * ایمنی در برابر انفجار
5. NPB 105-03 "تعیین دسته بندی محل ها و ساختمانها ، تاسیسات بیرونی برای انفجار و خطر آتش سوزی".
6. SNiP 23 -01-99 اقلیم شناسی ساخت و ساز.
7. خطر آتش سوزی و انفجار مواد و مواد و وسایل خاموش شدن آنها. اد A. N. Baratova و A. Ya. Korolchenko. م. ، شیمی ، 1990. 8. قوانین تاسیسات الکتریکی. اد هفتم
حرکت شعله از طریق مخلوط گازپخش شعله نامیده می شود. بسته به سرعت انتشار شعله ، احتراق می تواند تخلیه با سرعت چند متر بر ثانیه ، انفجاری - سرعت مرتب ده ها و صدها متر بر ثانیه و منفجر شدن - هزاران متر بر ثانیه باشد.
برای تخریب یا انتشار احتراق طبیعیانتقال حرارت از لایه ای به لایه مشخصه است و شعله ناشی از مخلوط گرم شده و رقیق شده با رادیکال های فعال و محصولات واکنش در جهت مخلوط قابل احتراق اولیه حرکت می کند. این به دلیل این واقعیت است که شعله ، به عنوان مثال ، به منبعی تبدیل می شود که جریان مداوم گرما و ذرات فعال شیمیایی را ساطع می کند. در نتیجه ، قسمت جلوی شعله به سمت مخلوط قابل احتراق حرکت می کند.
احتراق deflagrationبه لمینار و آشفته تقسیم می شود.
احتراق ورقه ای با سرعت انتشار شعله طبیعی مشخص می شود.
سرعت طبیعی انتشار شعله ، مطابق با GOST 12.1.044 SSBT ، نامیده می شود سرعت جلو شعلهگاز نسبتاً نسوخته ، در جهتی عمود بر سطح آن.
مقدار سرعت نرمال انتشار شعله ، به عنوان یکی از شاخص های آتش سوزی و انفجار مواد ، خطر صنایع مرتبط با استفاده از مایعات و گازها را مشخص می کند ، برای محاسبه میزان افزایش فشار انفجاری از آن استفاده می شود گاز ، مخلوط بخار هوا ، قطر بحرانی (خاموش کردن) و در توسعه اقدامات اطمینان از ایمنی در برابر آتش سوزی و انفجار فرآیندهای فن آوری مطابق با الزامات GOST 12.1.004 و GOST 12.1.010 SSBT.
سرعت نرمال انتشار شعله - ثابت فیزیکوشیمیایی مخلوط - به ترکیب مخلوط ، فشار و دما بستگی دارد و با سرعت واکنش شیمیایی و هدایت حرارتی مولکولی تعیین می شود.
دما نسبتاً ضعیف سرعت طبیعی انتشار شعله را افزایش می دهد ، ناخالصی های بی اثر آن را کاهش می دهند و افزایش فشار منجر به افزایش یا کاهش سرعت می شود.
در جریان گاز لایه ایسرعت گازها کم است و مخلوط قابل احتراق در نتیجه انتشار مولکولی تشکیل می شود. میزان سوختن در این حالت به سرعت تشکیل مخلوط قابل احتراق بستگی دارد. شعله آشفتهبا افزایش سرعت انتشار شعله ، هنگامی که لمینیتر حرکت آن نقض می شود ، تشکیل می شود. در یک شعله آشفته ، چرخش جت های گاز باعث بهبود اختلاط گازهای واکنش دهنده می شود ، زیرا سطحی که از طریق آن انتشار مولکولی رخ می دهد افزایش می یابد.
در نتیجه فعل و انفعال ماده قابل احتراق با اکسید کننده ، محصولات احتراق تشکیل می شود که ترکیب آنها به ترکیبات اولیه و شرایط واکنش احتراق بستگی دارد.
با احتراق کامل ترکیبات آلی ، CO 2 ، SO 2 ، H 2 O ، N 2 و با احتراق ترکیبات غیر آلی ، اکسیدها تشکیل می شوند. بسته به نقطه ذوب ، محصولات واکنش می توانند به صورت مذاب (Al 2 O 3 ، TiO 2) باشند یا به صورت دود به هوا بروند (P 2 O 5 ، Na 2 O ، MgO) . جامدات مذاب درخشندگی شعله را ایجاد می کنند. در احتراق هیدروکربن ها ، درخشندگی شدید شعله از طریق درخشش ذرات کربن فنی تأمین می شود که در مقادیر زیادی تشکیل می شود. کاهش محتوای کربن سیاه در نتیجه اکسیداسیون آن ، درخشندگی شعله را کاهش می دهد و کاهش دما اکسیداسیون کربن سیاه را دشوار می کند و منجر به تشکیل دوده در شعله می شود.
به منظور قطع واکنش احتراق ، لازم است شرایط وقوع و نگهداری آن را نقض کنید. معمولاً برای خاموش کردن ، از نقض دو شرط اساسی حالت پایدار استفاده می شود - کاهش دما و حالت حرکت گاز.
پایین آوردن دمابا معرفی موادی که در نتیجه تبخیر و تفکیک گرمای زیادی جذب می کنند (به عنوان مثال آب ، پودرها) می توان به دست آورد.
حالت حرکت گازبا کاهش و از بین بردن اکسیژن رسانی می توان تغییر کرد.
انفجار ، مطابق با GOST 12.1.010 " ایمنی در برابر انفجار"، - تحول سریع ماده (احتراق انفجاری) ، همراه با آزاد سازی انرژی و تشکیل گازهای فشرده شده قادر به انجام کار.
یک انفجار ، به عنوان یک قاعده ، منجر به افزایش شدید فشار می شود. یک موج شوک در محیط تولید و انتشار می یابد.
موج شوکاگر فشار اضافی در آن بیشتر از 15 کیلو پاسکال باشد ، ظرفیت تخریبی دارد. با سرعت صوتی 330 متر بر ثانیه در گاز جلوتر از جلوی شعله پخش می شود. در یک انفجار ، انرژی اولیه به انرژی گازهای فشرده شده گرم شده تبدیل می شود ، که به انرژی حرکت ، فشرده سازی و گرمایش محیط تبدیل می شود. انواع مختلفی از انرژی اولیه انفجار ممکن است - الکتریکی ، حرارتی ، انرژی فشرده سازی الاستیک ، اتمی ، شیمیایی.
پارامترهای اصلی توصیف کننده خطر انفجار مطابق با GOST 12.1.010 فشار در جلو شوک ، حداکثر فشار انفجار ، متوسط و حداکثر سرعت افزایش فشار در هنگام انفجار ، خرد کردن یا خاصیت انفجاری بالا در یک محیط منفجره است.
اقدام انفجار عمومیخود را در تخریب تجهیزات یا محل های ناشی از موج ضربه و همچنین در انتشار مواد مضر (محصولات انفجاری یا موجود در تجهیزات) نشان می دهد.
حداکثر فشار انفجار(حداکثر P) - بالاترین فشار ناشی از انفجار تخلیه مخلوط گاز ، بخار یا گرد و غبار هوا در یک ظرف بسته با فشار مخلوط اولیه 101.3 کیلو پاسکال.
سرعت افزایش فشار پشت سر هم(dР / dt) مشتق زمانی فشار انفجار در بخش صعودی وابستگی فشار انفجار مخلوط گاز ، بخار و هوا و غبار در ظرف بسته به موقع است. در همان زمان ، بین حداکثر و میانگین میزان افزایش فشار در هنگام انفجار تمایز قائل می شود. هنگام ایجاد حداکثر سرعت ، از افزایش فشار بر روی خط مستقیم فشار انفجار در برابر زمان و هنگام تعیین سرعت متوسط ، مقطع بین فشار حداکثر انفجار و فشار اولیه در ظرف قبل از انفجار استفاده می شود.
هر دوی این خصوصیات فاکتورهای مهمی برای اطمینان از محافظت در برابر انفجار هستند. آنها هنگام ایجاد دسته ای از محل ها و ساختمانها برای انفجار و خطر آتش سوزی ، هنگام محاسبه دستگاه های ایمنی ، هنگام ایجاد اقدامات برای ایمنی در برابر آتش سوزی و انفجار فرآیندهای فن آوری استفاده می شود.
انفجارفرآیند تبدیل شیمیایی سیستم اکسید کننده - عامل کاهش دهنده است که ترکیبی از یک موج شوک است که با سرعت ثابت و بیش از سرعت صدا پخش می شود و به دنبال قسمت جلوی منطقه تحولات شیمیایی مواد اولیه است. انرژی شیمیاییآزاد شده در موج انفجار موج شوک را تغذیه می کند و از میرایی آن جلوگیری می کند. سرعت موج انفجار مشخصه هر سیستم خاص است.
این تئوری می گوید که انفجار مخلوط گاز یا بخار هوا یک پدیده فوری نیست. هنگامی که منبع جرقه زنی به مخلوط قابل احتراق وارد می شود ، واکنش اکسیداسیون سوخت با اکسید کننده در ناحیه منبع احتراق آغاز می شود. سرعت واکنش اکسیداسیون در برخی از حجم اولیه این منطقه به حداکثر می رسد - احتراق رخ می دهد. احتراق در مرز حجم اولیه با محیط را شعله جلویی می نامند. جلوی شعله مانند یک کره است. ضخامت جلوی شعله ، محاسبه شده توسط Ya.B. زلدوویچ , برابر 1-100 میکرون است. اگرچه ضخامت ناحیه احتراق کم است ، اما برای ادامه واکنش احتراق کافی است. دمای جلوی شعله در اثر حرارت واکنش احتراق 1000-3000 درجه سانتیگراد است و به ترکیب مخلوط قابل احتراق بستگی دارد.
هنگامی که قسمت جلوی شعله حرکت می کند ، از آنجا که فشار مخلوط افزایش می یابد ، درجه حرارت قسمت نسوخته از مخلوط قابل احتراق افزایش می یابد. نزدیک شعله شعله ، دمای مخلوط نیز افزایش می یابد ، که ناشی از این است
انتقال گرما توسط هدایت حرارتی ، انتشار مولکول های گرم شده و تابش. در سطح خارجی قسمت جلوی شعله ، این دما برابر با دمای خود احتراق مخلوط قابل احتراق است.
بعد از احتراق مخلوط قابل احتراق ، شکل کروی شعله خیلی سریع تحریف شده و بیشتر و بیشتر به سمت مخلوطی که هنوز مشتعل نشده کشیده می شود. کشش جلوی شعله و افزایش سریع سطح آن با افزایش سرعت قسمت مرکزی شعله همراه است. این شتاب تا زمانی که شعله به دیواره های لوله ها نرسد یا در هر صورت به دیواره لوله نزدیک شود ادامه دارد. در این لحظه ، اندازه شعله به شدت کاهش می یابد و فقط قسمت کوچکی از شعله باقی می ماند و کل قسمت لوله را می پوشاند. بیرون کشیدن جلوی شعله
و شتاب شدید آن بلافاصله پس از اشتعال توسط جرقه ، هنگامی که شعله هنوز به دیواره های لوله نرسیده است ، ناشی از افزایش حجم محصولات احتراق است. بنابراین ، در مرحله اولیه روند تشکیل جبهه شعله ، بدون در نظر گرفتن میزان قابل احتراق مخلوط گاز ، شتاب و کاهش سرعت بعدی شعله اتفاق می افتد و این کاهش سرعت بیشتر خواهد بود ، سرعت شعله بیشتر خواهد بود.
توسعه مراحل بعدی احتراق تحت تأثیر طول لوله است. کشیدگی لوله منجر به ظهور ارتعاشات و تشکیل ساختار سلولی شعله ، شوک و انفجار امواج می شود.
عرض منطقه گرمایش (در سانتی متر) را می توان از وابستگی تعیین کرد
1 = a / v
جایی که ولی- ضریب نفوذ حرارتی ؛ v- سرعت انتشار شعله.
سرعت حرکت خطی v(در متر بر ثانیه) را می توان با فرمول تعیین کرد
V = V t /
جایی که V t- سرعت سوزاندن جرم ، گرم در (سانتی متر 3) ؛ - تراکم مخلوط قابل احتراق اولیه ، کیلوگرم در متر مکعب.
سرعت حرکت خطی جلوی شعله ثابت نیست ، بسته به ترکیبات تغییر می کند. مخلوط ها و ناخالصی های گازهای بی اثر (غیر قابل احتراق) ، دمای مخلوط ، قطر لوله و غیره. حداکثر سرعت انتشار شعله نه در غلظت استوکیومتری مخلوط ، بلکه در مخلوط با سوخت اضافی مشاهده می شود. وقتی گازهای بی اثر به مخلوط قابل احتراق وارد می شوند ، سرعت انتشار شعله کاهش می یابد. این امر با کاهش دمای احتراق مخلوط توضیح داده می شود ، زیرا بخشی از گرما صرف گرم کردن ناخالصی های بی اثر می شود که در واکنش شرکت نمی کنند.
با افزایش قطر لوله ها ، سرعت انتشار شعله به طور ناموزونی افزایش می یابد. با افزایش قطر لوله ها به 0.1-0.15 متر ، سرعت رشد سریع می کند. دما افزایش می یابد تا زمانی که قطر به یک قطر محدود خاص برسد ،
بالاتر از آن هیچ افزایشی در سرعت وجود ندارد. با کاهش قطر لوله ، سرعت انتشار شعله کاهش می یابد و در یک قطر کوچک خاص ، شعله در لوله گسترش نمی یابد. این پدیده را می توان با افزایش تلفات گرما از طریق دیواره ها توضیح داد.
لوله های.
بنابراین ، برای جلوگیری از انتشار شعله در مخلوط قابل احتراق ، لازم است که دمای مخلوط را به یک روش یا دیگری کاهش دهید ، با خنک کردن ظرف (در مثال ما یک لوله) از خارج یا با رقیق کردن مخلوط با یک گاز بی اثر سرد.
سرعت نرمال انتشار شعله نسبتاً کم است (بیش از ده متر در ثانیه) ، اما تحت برخی شرایط ، شعله در لوله ها با سرعت فوق العاده (از 2 تا 5 کیلومتر در ثانیه) گسترش می یابد ، بیش از سرعت صدا در یک محیط معین این پدیده نامگذاری شد انفجار... ویژگی های متمایز انفجار به شرح زیر است:
1) نرخ سوختن ثابت بدون توجه به قطر لوله ؛
2) فشار شعله بالا ناشی از موج انفجار ، که می تواند بیش از 50 مگاپاسکال باشد ، بسته به ماهیت شیمیایی مخلوط قابل احتراق و فشار اولیه ؛ علاوه بر این ، به دلیل سرعت بالا در سوزاندن ، فشار ایجاد شده به شکل ، ظرفیت و فشردگی رگ (یا لوله) بستگی ندارد.
با شتاب گرفتن شعله ، دامنه موج شوک نیز افزایش می یابد ، دمای فشرده سازی به دمای خود روشن شدن مخلوط می رسد.
افزایش مقدار کل احتراق گاز در واحد زمان با این واقعیت توضیح داده می شود که در یک جت با سرعت مقطع متغیر ، قسمت جلوی شعله خم می شود ، در نتیجه سطح آن افزایش می یابد و مقدار ماده قابل احتراق به طور متناسب افزایش می یابد .
هنگامی که مخلوط های گاز در حجم بسته می سوزند ، محصولات احتراق کار نمی کنند. انرژی انفجار فقط برای گرم کردن محصولات انفجار صرف می شود. در این حالت ، کل انرژی به عنوان مجموع انرژی داخلی مخلوط انفجاری Q vn.en.cm تعیین می شود. و گرمای احتراق یک ماده معین ΔQ گرم. مقدار Q int.en.cm. برابر است با مجموع محصولات ظرفیت گرمایی اجزای مخلوط مواد منفجره در حجم ثابت توسط دمای اولیه
دمای مخلوط
Q int.en. سانتی متر = C 1 T + C 2 T + ... + C p T
جایی که C 1 ، C 2 ، C p ظرفیت گرمایی ویژه اجزای سازنده است
مخلوط انفجاری ، kJ / (کیلوگرم کیلوگرم) ؛ T -دمای اولیه مخلوط ، K
دمای انفجار مخلوط های گاز در حجم ثابت با همان روش دمای احتراق مخلوط در فشار ثابت محاسبه می شود.
فشار انفجار از دمای انفجار پیدا می شود. فشار حین انفجار مخلوط گاز و هوا در حجم بسته به دمای انفجار و نسبت تعداد مولکول های محصولات احتراق به تعداد مولکول های مخلوط انفجاری بستگی دارد. اگر فشار اولیه مخلوط نرمال باشد ، در انفجار مخلوط های گاز و هوا ، فشار معمولاً از 1.0 مگاپاسکال بیشتر نمی شود. هنگام جایگزینی هوا در مخلوط انفجاری با اکسیژن ، از آنجا که دمای احتراق افزایش می یابد ، فشار انفجار به شدت افزایش می یابد.
فشار انفجار مخلوط استوکیومتری متان ، اتیلن ، استون و
متیل اتر با اکسیژن 1.5 - 1.9 مگاپاسکال است و مخلوط استوکیومتری آنها با هوا 1.0 مگاپاسکال است.
حداکثر فشار انفجار در محاسبات مقاومت در برابر انفجار تجهیزات و همچنین در محاسبات دریچه های ایمنی ، غشاهای انفجار و محفظه های تجهیزات الکتریکی ضد انفجار استفاده می شود. فشار پشت سر هم Rمخلوط های گاز و هوا vzr (در MPa) با فرمول محاسبه می شوند
Rبزرگسال =
جایی که ص 0- فشار اولیه مخلوط انفجاری ، MPa ؛ T 0و T بزرگسال- دمای اولیه مخلوط انفجاری و دمای انفجار ، K ؛
تعداد مولکولهای گازهای احتراق پس از انفجار ؛
- تعداد مولکولهای گازهای مخلوط قبل از انفجار.
 چه کسی و چگونه پول خود را در جایگزینی واردات و نوآوری در کشاورزی می گیرد R
چه کسی و چگونه پول خود را در جایگزینی واردات و نوآوری در کشاورزی می گیرد R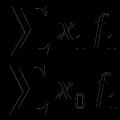 شاخص تولید صنعتی ، نقش و محاسبه آن چیست
شاخص تولید صنعتی ، نقش و محاسبه آن چیست محاسبه جمعیت طراحی شهر اصطلاح در متالورژی
محاسبه جمعیت طراحی شهر اصطلاح در متالورژی